【关于细胞治疗】
细胞治疗是指将正常或经过基因工程改造的人体细胞输入患者体内,新输入的细胞可以替代受损细胞或者具有更强的免疫杀伤功能,从而达到治疗疾病的目的。细胞疗法在治疗肿瘤(包括实体瘤和血液瘤)、自免疾病等方面显示出越来越高的应用价值。一般来讲,细胞治疗包括免疫细胞治疗和干细胞治疗。
免疫细胞治疗主要包括了T细胞治疗、NK细胞治疗、淋巴细胞治疗、DC细胞治疗。干细胞治疗包括了多能诱导干细胞疗法,也包括了间充质干细胞、造血干细胞、神经干细胞等其他干细胞疗法。
在肿瘤治疗和自免疾病治疗领域,近些年来不断取得技术突破并走向商业化的产品,主要集中于免疫细胞治疗和以多能诱导干细胞为来源的免疫细胞疗法。包括了CAR-T疗法、TCR-T疗法、CAR-NK疗法、TIL疗法,DC细胞治疗也有所发展。近年来,不仅自体CAR-T疗法有多款产品获批上市,通用型CAR-T疗法,也有了突破性的发展成果。
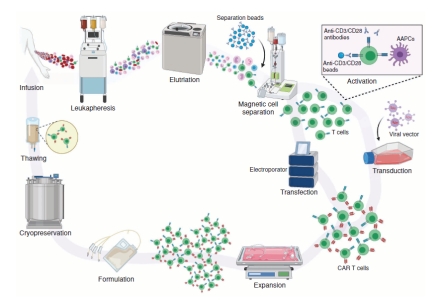
Abou-El-Enein et al. Blood Cancer Discov. 2021
【已上市的细胞治疗疗法】
产品 | 生产商 | 靶点 | 疗法 | 适应症 | 上市时间 |
Kymriah | 诺华 | CD19 | CAR-T | DLBCL/B-ALL | 2017 |
Yescarta | Gilead/Kite | CD19 | CAR-T | DLBCL/FL | 2017 |
Tecartus | Gilead/Kite | CD19 | CAR-T | DLBCL/B-ALL | 2021 |
Breyanzi | BMS/Juno/药明 | CD19 | CAR-T | DLBCL/MZL | 2021 |
Abecma | BMS/Bluebird | BCMA | CAR-T | MM | 2021 |
Carvykti | 传奇 | BCMA | CAR-T | MM | 2022 |
tebentafusp | Kimmtrak | gp100 | TCR-T | 转移性葡萄膜黑色素瘤 | 2022 |
tabelecleucel | Atara Bio | EBV ag | CAR-T | EBV阳性移植后淋巴增殖性疾病(PTLD) | phase III |
伊基奥仑赛 | 驯鹿 | BCMA | CAR-T | MM | 2023 |
泽沃基奥仑赛 | 科挤 | BCMA | CAR-T | MM | 2024 |
雷尼基奥仑赛 | 恒润达生 | CD19 | CAR-T | DLBCL | 2025 |
舒瑞基奥仑赛 | 科挤 | Claudin 18.2 | CAR-T | 胃/食管胃结合部腺癌(G/GEJA) | phase II |
已经商业化和即将商业化的产品主要集中于自体免疫细胞治疗,其中CAR-T占了大多数,TCR-T和CAR-NK产品也多有进展靠前的产品。
【CAR-T和TCR-T疗法】
I.T细胞改造方法
两种针对T细胞开展工程改造,提升其特异性杀伤肿瘤细胞效果的治疗技术。基于HIV-1的慢病毒载体因其感染T细胞的能力,成为了改造T细胞的有效载体。在多年工艺探索后,慢病毒稳转体系目前是T细胞改造的主流方法,T细胞改造质量可靠且稳定,形成了相对可控的工艺体系。工艺所涉原料详见文末原料列表。
II. CAR结构与肿瘤杀伤
CAR-T细胞治疗,即嵌合抗原受体T细胞治疗,是将人的T细胞经过基因工程手段体外修饰改造后,回输患者体内。改造后的T细胞,可识别体内肿瘤细胞,并通过免疫作用释放大量的多种效应因子,它们能高效地杀灭肿瘤细胞,从而达到治疗恶性肿瘤的目的。
对T细胞的改造主要是进行CAR分子的“安装”。CAR(嵌合抗原受体)是抗体的抗原结合区 scFv 与 CD3-ζ 链或 FcεRIγ 的胞内部分进行融合形成,是 CAR-T 的核心部件。与TCR介导的抗原识别相比,CAR的抗原识别并不依赖于主要的组织相容性复合体(MHC),改造成功的CAR-T细胞可直接通过CAR分子识别特异性抗原。
CAR结构通常也由三部分组成,即胞外抗原结合区(一般为scFv)、跨膜结构域以及胞内激活结构域。经过多年发展,CAR结构已经发展至第四第五代,CAR结构的改进主要集中在胞内共刺激结构域。有学者在第四代CAR-T的设计中添加细胞因子或趋化因子受体结构,从而增加T细胞在肿瘤组织中的浸润,达到增强杀伤实体瘤的效果。第五代CAR在共刺激域(如CD28或4-1BB)和CD3ζ链之间,插入了IL-2Rβ等细胞因子受体的胞内片段,当CAR结合抗原后,该片段包含的YXXQ基序(Y代表酪氨酸)招募并激活JAK激酶和STAT蛋白,从而同时启动T细胞活化和细胞因子驱动的增殖信号。
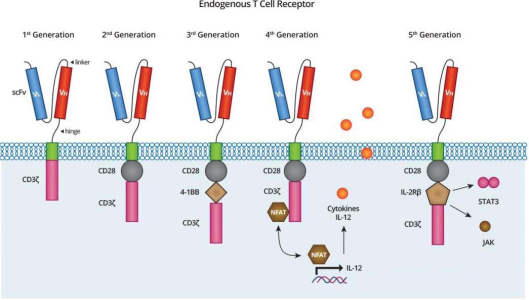
CAR结构示意图
III. TCR结构与肿瘤杀伤
TCR-T疗法依赖T细胞受体(TCR)与MHC呈递的胞内抗原结合识别肿瘤细胞。MHC有两种类型MHC-I与MHC-II,由人类6号染色体短臂上的人类白细胞抗原(HLA)基因座编码,在细胞表面不同程度表达。其中,HLA-A、HLA-B及HLA-C编码MHC-I型分子,HLA-DR、HLA-DQ、HLA-DP编码MHC-II型分子。MHC-I负责呈递内源性抗原信号分子,它在几乎所有有核细胞表面表达,由一条α链和β球蛋白组成,其中α1和α2两个结构域构成一个沟(Groove),这是肽段结合区,其允许抗原多肽片段结合并呈递到细胞膜表面。MHC-II负责呈递外源性信号分子,在抗原呈递细胞(APC)表面表达,如单核-巨噬细胞、树突状细胞及B细胞等。MHC-II由α和β两条链组成,其中α1与β1之间形成的沟能参与抗原多肽片段的结合。
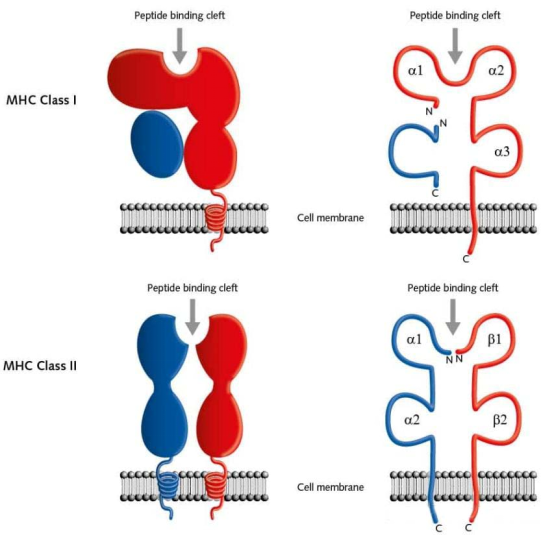
MHC结构示意图
内源性抗原是细胞自身产生的蛋白,如病毒感染后利用宿主细胞合成的蛋白质外壳或癌变的肿瘤蛋白。在细胞内,这些内源性蛋白在被自身细胞处理后会形成小分子肽段,然后与MHC-I结合形成pMHC-I复合物,并被呈递到细胞膜表面与CD8+ T细胞结合,从而介导细胞的凋亡或程序性死亡。TCR-T细胞的激活也依赖于CD3分子的信号传导,依赖于各个亚基的免疫受体络氨酸活化基序(ITAM)磷酸化实现。
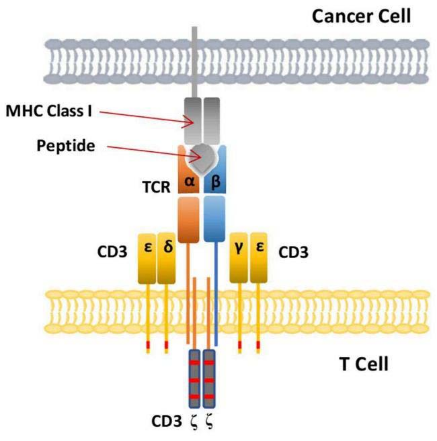
TCR与pMHC结合
TCR-T与CAR-T都是经基因工程改造的T细胞,使其具有特异识别并清除肿瘤的能力,然后回输到体内以达到治疗癌症的目的。CAR-T识别的靶抗原都是细胞表面蛋白,这些靶蛋白的数量是有限的。TCR-T可以识别MHC分子呈递的细胞内多肽片段,因此TCR-T的靶抗原范围更广。TCR-T的技术核心是修饰TCR与肿瘤抗原的结合,人体内天然的TCR对这些抗原的亲和力相对较低,因此无法识别和杀死肿瘤细胞。人工设计的高亲和力TCR在识别肿瘤细胞的过程中增强了特异性识别和亲和力。
TCR-T治疗是依赖于MHC分子的呈递来识别和激活T细胞,这也是TCR-T的缺点。MHC由HLA基因编码,该基因是人类基因组中多态性最强的基因。在接受TCR-T治疗的患者不仅必须表达靶向抗原,还必须表达相应的HLA等位基因抗原。因此,TCR-T疗法通常使用仅限于相对常见的HLA等位基因的TCR。
【T细胞培养工艺】
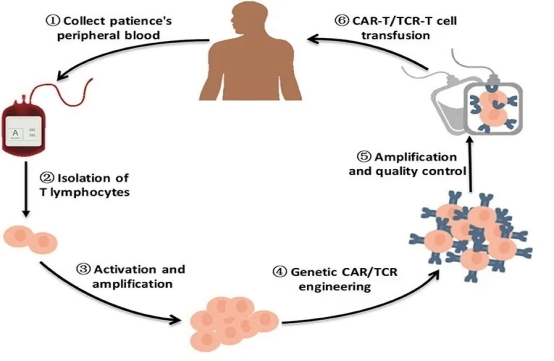
CAR-T/TCR-T Therapeutics
早先CIK细胞培养中,很多人忽略CD28抗体对T细胞活化及防止T细胞失能的效果。T细胞的有效活化依赖于TCR途径的激活和共刺激信号特别是CD28信号途径的激活。
依靠IL-2的传统培养中,激活扩增得到的T细胞中,完全分化的效应T细胞(TEF)占比更多。在使用IL-15部分替代IL-2的培养中,未完全分化的记忆T细胞(Tscm)的占比较仅以IL-2的显著的多,研究表明,T细胞亚群的选择是CAR-T细胞治疗效果的基础。在这方面,中央记忆T细胞(TCM)的CAR转导似乎对体内有效的细胞扩张、存活和持久性至关重要,同样数量细胞移植,移植Tscm的子代细胞数量较Tcm高10~100倍(Gattinoni L, Nat. Med.,2011)。此外,选择幼稚或分化程度较低的CD8+T细胞进行转导可以使输注后T细胞增殖和体内持久性增加。
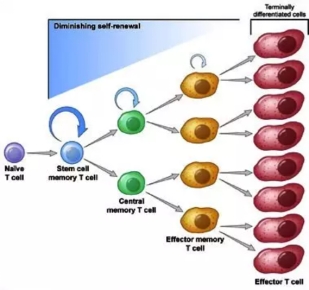
T细胞的分化
Hopkins B等人进行了一项实验设计,研究不同组合IL-2、IL-7、IL-15对T细胞亚群生长的影响。结果表明,CD4+和CD8+ naïve T细胞分别在中等浓度的IL-2和IL-7组合以及IL-7作用下可以有效生长。CD4+和CD8+记忆细胞分别在中等浓度IL-2和IL-15组合以及中等浓度IL-7和IL-15组合中有利。Coppola C等研究结果表明IL-2和IL-7在促进活化的CD4+ T细胞的最佳增殖和存活方面存在协同作用。
【NK细胞与CAR-NK】
I.NK细胞杀伤机制
与T细胞的杀伤作用机制不同,NK细胞的杀伤活性受细胞表面的抑制性受体和激活性受体的共同调控,当激活与抑制的平衡被打破,NK细胞便会行使相应的功能。
具体来讲,NK细胞表面的抑制性受体(主要是抑制性杀伤性Ig样受体KIRs和异二聚体C型凝集素受体NKG2A)可与靶细胞表面的MHC I结合并传递抑制信号,从而使NK细胞进入“沉默”状态;而NK细胞表面的激活性受体(主要是NCRs、NKp46、NKp30、NKp44和NKG2D)与可与细胞表面的特异性激活配体结合,从而激活NK细胞。
NK细胞主要通过三种机制杀伤靶细胞:
1. 通过释放含有穿孔素和颗粒酶的细胞质颗粒直接杀伤靶细胞
2. 释放细胞因子,如IFN-γ、TNF-α等,通过与肿瘤细胞表面相应受体的相互作用诱导肿瘤细胞凋亡。
3. Fc受体CD16与抗体的Fc段结合,可激发抗体依赖的细胞介导的细胞毒性(ADCC)来杀伤细胞。
生理情况下,NK细胞抑制性受体识别正常组织细胞表面广泛表达的MHC-Ⅰ类分子而使NK细胞功能受到抑制,无法杀伤自身正常组织细胞。在肿瘤组织中,一方面肿瘤细胞表面MHC-Ⅰ类分子表达通常发生下调,另一方面活化受体的配体如NKp30、NKp44、NKp46等表达上调,这两方面的因素将导致NK细胞活化最终杀伤肿瘤细胞。
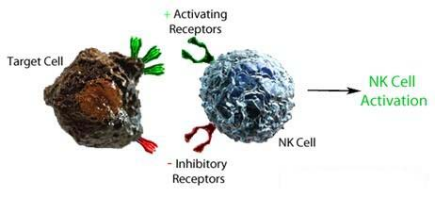
NK细胞的抑制和激活
II.CAR-NK的CAR结构
CAR-NK细胞的CAR结构通常也由三部分组成,这与CAR-T细胞疗法中使用的CAR结构十分类似,事实上,目前的很多研究直接是把CAR-T中成熟的CAR结构在NK细胞系中表达来制备CAR-NK。与CAR-T中常见的CAR结构相比,CAR-NK还可以选择NKG2D作为CAR结构的识别结构域,原因是肿瘤中普遍发生NKG2D的配体NKG2DL表达的上调。
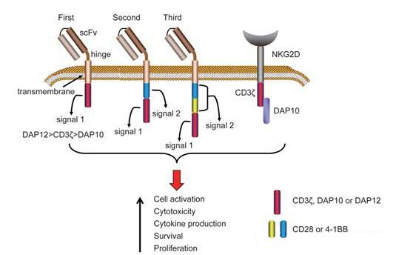
CAR-NK的CAR结构
III.NK细胞转染改造
不同于HIV-1病毒改造后的慢病毒载体感染T细胞,NK细胞缺乏高效的慢病毒载体。目前,主要采用瞬转工艺作为生产工艺。
【NK细胞培养工艺】
I.使用细胞因子培养NK细胞
细胞因子是维持NK细胞存活和支持NK细胞体外增殖的关键成分,可以不需要滋养细胞的条件下培养细胞。然而,当使用不同的细胞因子和培养条件时,发现具有不同的扩增效率。
除了仅使用细胞因子的策略外,还有细胞因子和饲养细胞联合使用的策略,饲养细胞包括照射的肿瘤细胞、同种异体PBMCs和淋巴母细胞衍生物等。缺乏人类白细胞抗原表达的K562细胞能通过激活共刺激信号促进NK细胞的增殖,据报道,当K562细胞作为饲养细胞与IL-2和IL-15联合使用时,NK细胞的扩增超过300倍。
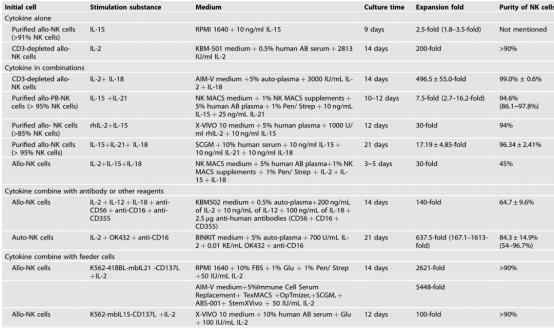
一些PBMC来源NK细胞的扩增方法
肿瘤细胞膜颗粒也是肿瘤细胞系扩增NK细胞的有效替代品,其不仅保持了诱导NK细胞扩增的膜受体的激活效率,而且避免了肿瘤细胞与扩增产物混合的风险。
新的无饲养层扩张系统正在开发中,细胞因子如IL-2、IL-15和IL-21的单一或简单组合被用于扩增细胞。细胞因子、链球菌和唑来膦酸盐刺激脐血单个核细胞3周,可产生平均纯度为95%的NK细胞,扩增倍数可达1561倍。这种无饲养层的方法降低了将其他类型的细胞引入最终产品的风险,但NK细胞的纯度仍需提高。
II.NK细胞系
NK-92是第一个获得FDA批准用于临床试验的基于NK细胞的细胞系,是一种同质的永生化NK淋巴瘤细胞系,可以在体外扩增以获得大量细胞。NK-92细胞表面标志CD56和CD25阳性,CD3、CD4、CD8、CD16、CD32、CD64和HLA-DR阴性。NK-92细胞的生长依赖于IL-2。由于其致癌特性,需要在患者给药之前对NK-92衍生细胞产品进行辐射,这反过来又对其在体内的长期持久性和整体治疗潜力产生负面影响。另一个缺点是,由于缺乏CD16的表达,NK-92细胞缺乏通过ADCC介导细胞杀伤的能力。
【CAR-NK的比较优势】
不同于T细胞,NK细胞的一大独特之处在于,并不局限于自体细胞,目前的临床研究显示CAR-NK细胞不会产生GvHD(移植物抗宿主病),因此安全性较高。同种异体CAR-NK获取方便,质量均一且时效高,副作用小。
【相关产品列表】
细胞分离
品牌 | 货号 | 产品名称 |
Seebio | ACJ0020A | Polysucrose 400 聚蔗糖400 |
血清
品牌 | 货号 | 产品名称 | 规格 |
Seebio | EEM0020D | 优级胎牛血清 | 500ml |
Seebio | EBM0084A | 小牛血清 | 100ml、500ml |
Seebio | DDJ0002B | 特级新生牛血清 | 100ml |
细胞因子
货号 | 产品名称 | 包装规格 |
EDQ0056A | 重组人 BMP-2(rhBMP-2) | 50ug、1mg |
EDQ0057A | 重组人 BMP-4(rhBMP-4) | 50ug、1mg |
EDQ0058A | 重组人 BMP-7(rhBMP-7) | 10ug、50ug、1mg |
EDQ0061A | 重组人表皮生长因子(rhEGF) | 10ug、50ug、1mg |
EDQ0083A | 重组人 Noggin(rhNoggin) | 50ug、1mg |
EDQ0086A | 重组人 R-spondin(rhR-spondin) | 50ug、1mg |
EDQ0092A | 重组人 Wnt-3α(rhWnt-3α) | 50ug、1mg |
EDQ0106A | 重组人白细胞介素-2(rhIL-2) | 100ug、1mg |
EDQ0112A | 重组人白细胞介素-15(rhIL-15) | 50ug、1mg |
EDQ0113A | 重组人白细胞介素-17(rhIL-17) | 50ug、1mg |
EDQ0115A | 重组人白细胞介素-21(rhIL-21) | 50ug、100μg、1mg |
EDQ0096A | 重组人粒细胞集落刺激因子(rhG-CSF) | 1mg |
EDQ0097A | 重组人粒细胞巨噬细胞刺激因子(rhGM-CSF) | 100ug、1mg |
细胞抗结团 & 表面活性剂 & 消泡剂
品牌 | 货号 | 产品名称 | 规格 |
Seebio | DCJ0018D | 硫酸葡聚糖 5000(DSS),低内毒素 | 1g、25g、100g、500g |
Seebio | DCJ1606D | Seebio® 硫酸葡聚糖钠盐 40,000(DSS),低内毒素 | 1g、25g、100g、500g |
Seebio | DCH0535A | Seebio® P188 非离子表面活性剂(100×) | 50ml |
Seebio | ACH0497B | 泊洛沙姆188(药用级) | 1kg、20kg |
Seebio | DGF6890 | 亚油酸钠 | 1kg、25kg |
Seebio | ABY0110A | 金精三羧酸铵盐 | 50g、100g、500g |
Seebio | ACH0558A | 有机硅消泡剂 | 25g、100g、500g |
Seebio | ACH0476A-500g | 非离子型T-F复合型发酵用消泡剂 | 500g |
ITS添加剂原料
品牌 | 货号 | 产品名称 | 规格 |
Seebio | EYY3311 | 重组人胰岛素 | 1g |
Seebio | DBM0012 | 转铁蛋白 | 100mg、500mg、1g |
Seebio | DCL0001 | 牛血清白蛋白 | 1g、5g、25g、1kg |
Seebio | AJL0068 | 丙酮酸钠 | 1kg、25kg |
Seebio | EDQ0163A | 胎球蛋白A(FetuinA) | 100mg |
Seebio | EDQ0165A | 纤连蛋白(Fibronectin) | 10ug、50ug |
细胞冻存
品牌 | 货号 | 产品名称 | 规格 |
Seebio | AJL0007A | 二甲基亚砜(DMSO) | 500ml,4L |
wako | 302-14686 | BAMBANKER冻存液 | 100 mL |
wako | 306-14684 | BAMBANKER冻存液 | 20 mLx5 |
【关于细胞治疗】
细胞治疗是指将正常或经过基因工程改造的人体细胞输入患者体内,新输入的细胞可以替代受损细胞或者具有更强的免疫杀伤功能,从而达到治疗疾病的目的。细胞疗法在治疗肿瘤(包括实体瘤和血液瘤)、自免疾病等方面显示出越来越高的应用价值。一般来讲,细胞治疗包括免疫细胞治疗和干细胞治疗。
免疫细胞治疗主要包括了T细胞治疗、NK细胞治疗、淋巴细胞治疗、DC细胞治疗。干细胞治疗包括了多能诱导干细胞疗法,也包括了间充质干细胞、造血干细胞、神经干细胞等其他干细胞疗法。
在肿瘤治疗和自免疾病治疗领域,近些年来不断取得技术突破并走向商业化的产品,主要集中于免疫细胞治疗和以多能诱导干细胞为来源的免疫细胞疗法。包括了CAR-T疗法、TCR-T疗法、CAR-NK疗法、TIL疗法,DC细胞治疗也有所发展。近年来,不仅自体CAR-T疗法有多款产品获批上市,通用型CAR-T疗法,也有了突破性的发展成果。

Abou-El-Enein et al. Blood Cancer Discov. 2021
【已上市的细胞治疗疗法】
产品 | 生产商 | 靶点 | 疗法 | 适应症 | 上市时间 |
Kymriah | 诺华 | CD19 | CAR-T | DLBCL/B-ALL | 2017 |
Yescarta | Gilead/Kite | CD19 | CAR-T | DLBCL/FL | 2017 |
Tecartus | Gilead/Kite | CD19 | CAR-T | DLBCL/B-ALL | 2021 |
Breyanzi | BMS/Juno/药明 | CD19 | CAR-T | DLBCL/MZL | 2021 |
Abecma | BMS/Bluebird | BCMA | CAR-T | MM | 2021 |
Carvykti | 传奇 | BCMA | CAR-T | MM | 2022 |
tebentafusp | Kimmtrak | gp100 | TCR-T | 转移性葡萄膜黑色素瘤 | 2022 |
tabelecleucel | Atara Bio | EBV ag | CAR-T | EBV阳性移植后淋巴增殖性疾病(PTLD) | phase III |
伊基奥仑赛 | 驯鹿 | BCMA | CAR-T | MM | 2023 |
泽沃基奥仑赛 | 科挤 | BCMA | CAR-T | MM | 2024 |
雷尼基奥仑赛 | 恒润达生 | CD19 | CAR-T | DLBCL | 2025 |
舒瑞基奥仑赛 | 科挤 | Claudin 18.2 | CAR-T | 胃/食管胃结合部腺癌(G/GEJA) | phase II |
已经商业化和即将商业化的产品主要集中于自体免疫细胞治疗,其中CAR-T占了大多数,TCR-T和CAR-NK产品也多有进展靠前的产品。
【CAR-T和TCR-T疗法】
I.T细胞改造方法
两种针对T细胞开展工程改造,提升其特异性杀伤肿瘤细胞效果的治疗技术。基于HIV-1的慢病毒载体因其感染T细胞的能力,成为了改造T细胞的有效载体。在多年工艺探索后,慢病毒稳转体系目前是T细胞改造的主流方法,T细胞改造质量可靠且稳定,形成了相对可控的工艺体系。工艺所涉原料详见文末原料列表。
II. CAR结构与肿瘤杀伤
CAR-T细胞治疗,即嵌合抗原受体T细胞治疗,是将人的T细胞经过基因工程手段体外修饰改造后,回输患者体内。改造后的T细胞,可识别体内肿瘤细胞,并通过免疫作用释放大量的多种效应因子,它们能高效地杀灭肿瘤细胞,从而达到治疗恶性肿瘤的目的。
对T细胞的改造主要是进行CAR分子的“安装”。CAR(嵌合抗原受体)是抗体的抗原结合区 scFv 与 CD3-ζ 链或 FcεRIγ 的胞内部分进行融合形成,是 CAR-T 的核心部件。与TCR介导的抗原识别相比,CAR的抗原识别并不依赖于主要的组织相容性复合体(MHC),改造成功的CAR-T细胞可直接通过CAR分子识别特异性抗原。
CAR结构通常也由三部分组成,即胞外抗原结合区(一般为scFv)、跨膜结构域以及胞内激活结构域。经过多年发展,CAR结构已经发展至第四第五代,CAR结构的改进主要集中在胞内共刺激结构域。有学者在第四代CAR-T的设计中添加细胞因子或趋化因子受体结构,从而增加T细胞在肿瘤组织中的浸润,达到增强杀伤实体瘤的效果。第五代CAR在共刺激域(如CD28或4-1BB)和CD3ζ链之间,插入了IL-2Rβ等细胞因子受体的胞内片段,当CAR结合抗原后,该片段包含的YXXQ基序(Y代表酪氨酸)招募并激活JAK激酶和STAT蛋白,从而同时启动T细胞活化和细胞因子驱动的增殖信号。

CAR结构示意图
III. TCR结构与肿瘤杀伤
TCR-T疗法依赖T细胞受体(TCR)与MHC呈递的胞内抗原结合识别肿瘤细胞。MHC有两种类型MHC-I与MHC-II,由人类6号染色体短臂上的人类白细胞抗原(HLA)基因座编码,在细胞表面不同程度表达。其中,HLA-A、HLA-B及HLA-C编码MHC-I型分子,HLA-DR、HLA-DQ、HLA-DP编码MHC-II型分子。MHC-I负责呈递内源性抗原信号分子,它在几乎所有有核细胞表面表达,由一条α链和β球蛋白组成,其中α1和α2两个结构域构成一个沟(Groove),这是肽段结合区,其允许抗原多肽片段结合并呈递到细胞膜表面。MHC-II负责呈递外源性信号分子,在抗原呈递细胞(APC)表面表达,如单核-巨噬细胞、树突状细胞及B细胞等。MHC-II由α和β两条链组成,其中α1与β1之间形成的沟能参与抗原多肽片段的结合。

MHC结构示意图
内源性抗原是细胞自身产生的蛋白,如病毒感染后利用宿主细胞合成的蛋白质外壳或癌变的肿瘤蛋白。在细胞内,这些内源性蛋白在被自身细胞处理后会形成小分子肽段,然后与MHC-I结合形成pMHC-I复合物,并被呈递到细胞膜表面与CD8+ T细胞结合,从而介导细胞的凋亡或程序性死亡。TCR-T细胞的激活也依赖于CD3分子的信号传导,依赖于各个亚基的免疫受体络氨酸活化基序(ITAM)磷酸化实现。

TCR与pMHC结合
TCR-T与CAR-T都是经基因工程改造的T细胞,使其具有特异识别并清除肿瘤的能力,然后回输到体内以达到治疗癌症的目的。CAR-T识别的靶抗原都是细胞表面蛋白,这些靶蛋白的数量是有限的。TCR-T可以识别MHC分子呈递的细胞内多肽片段,因此TCR-T的靶抗原范围更广。TCR-T的技术核心是修饰TCR与肿瘤抗原的结合,人体内天然的TCR对这些抗原的亲和力相对较低,因此无法识别和杀死肿瘤细胞。人工设计的高亲和力TCR在识别肿瘤细胞的过程中增强了特异性识别和亲和力。
TCR-T治疗是依赖于MHC分子的呈递来识别和激活T细胞,这也是TCR-T的缺点。MHC由HLA基因编码,该基因是人类基因组中多态性最强的基因。在接受TCR-T治疗的患者不仅必须表达靶向抗原,还必须表达相应的HLA等位基因抗原。因此,TCR-T疗法通常使用仅限于相对常见的HLA等位基因的TCR。
【T细胞培养工艺】

CAR-T/TCR-T Therapeutics
早先CIK细胞培养中,很多人忽略CD28抗体对T细胞活化及防止T细胞失能的效果。T细胞的有效活化依赖于TCR途径的激活和共刺激信号特别是CD28信号途径的激活。
依靠IL-2的传统培养中,激活扩增得到的T细胞中,完全分化的效应T细胞(TEF)占比更多。在使用IL-15部分替代IL-2的培养中,未完全分化的记忆T细胞(Tscm)的占比较仅以IL-2的显著的多,研究表明,T细胞亚群的选择是CAR-T细胞治疗效果的基础。在这方面,中央记忆T细胞(TCM)的CAR转导似乎对体内有效的细胞扩张、存活和持久性至关重要,同样数量细胞移植,移植Tscm的子代细胞数量较Tcm高10~100倍(Gattinoni L, Nat. Med.,2011)。此外,选择幼稚或分化程度较低的CD8+T细胞进行转导可以使输注后T细胞增殖和体内持久性增加。

T细胞的分化
Hopkins B等人进行了一项实验设计,研究不同组合IL-2、IL-7、IL-15对T细胞亚群生长的影响。结果表明,CD4+和CD8+ naïve T细胞分别在中等浓度的IL-2和IL-7组合以及IL-7作用下可以有效生长。CD4+和CD8+记忆细胞分别在中等浓度IL-2和IL-15组合以及中等浓度IL-7和IL-15组合中有利。Coppola C等研究结果表明IL-2和IL-7在促进活化的CD4+ T细胞的最佳增殖和存活方面存在协同作用。
【NK细胞与CAR-NK】
I.NK细胞杀伤机制
与T细胞的杀伤作用机制不同,NK细胞的杀伤活性受细胞表面的抑制性受体和激活性受体的共同调控,当激活与抑制的平衡被打破,NK细胞便会行使相应的功能。
具体来讲,NK细胞表面的抑制性受体(主要是抑制性杀伤性Ig样受体KIRs和异二聚体C型凝集素受体NKG2A)可与靶细胞表面的MHC I结合并传递抑制信号,从而使NK细胞进入“沉默”状态;而NK细胞表面的激活性受体(主要是NCRs、NKp46、NKp30、NKp44和NKG2D)与可与细胞表面的特异性激活配体结合,从而激活NK细胞。
NK细胞主要通过三种机制杀伤靶细胞:
1. 通过释放含有穿孔素和颗粒酶的细胞质颗粒直接杀伤靶细胞
2. 释放细胞因子,如IFN-γ、TNF-α等,通过与肿瘤细胞表面相应受体的相互作用诱导肿瘤细胞凋亡。
3. Fc受体CD16与抗体的Fc段结合,可激发抗体依赖的细胞介导的细胞毒性(ADCC)来杀伤细胞。
生理情况下,NK细胞抑制性受体识别正常组织细胞表面广泛表达的MHC-Ⅰ类分子而使NK细胞功能受到抑制,无法杀伤自身正常组织细胞。在肿瘤组织中,一方面肿瘤细胞表面MHC-Ⅰ类分子表达通常发生下调,另一方面活化受体的配体如NKp30、NKp44、NKp46等表达上调,这两方面的因素将导致NK细胞活化最终杀伤肿瘤细胞。

NK细胞的抑制和激活
II.CAR-NK的CAR结构
CAR-NK细胞的CAR结构通常也由三部分组成,这与CAR-T细胞疗法中使用的CAR结构十分类似,事实上,目前的很多研究直接是把CAR-T中成熟的CAR结构在NK细胞系中表达来制备CAR-NK。与CAR-T中常见的CAR结构相比,CAR-NK还可以选择NKG2D作为CAR结构的识别结构域,原因是肿瘤中普遍发生NKG2D的配体NKG2DL表达的上调。

CAR-NK的CAR结构
III.NK细胞转染改造
不同于HIV-1病毒改造后的慢病毒载体感染T细胞,NK细胞缺乏高效的慢病毒载体。目前,主要采用瞬转工艺作为生产工艺。
【NK细胞培养工艺】
I.使用细胞因子培养NK细胞
细胞因子是维持NK细胞存活和支持NK细胞体外增殖的关键成分,可以不需要滋养细胞的条件下培养细胞。然而,当使用不同的细胞因子和培养条件时,发现具有不同的扩增效率。
除了仅使用细胞因子的策略外,还有细胞因子和饲养细胞联合使用的策略,饲养细胞包括照射的肿瘤细胞、同种异体PBMCs和淋巴母细胞衍生物等。缺乏人类白细胞抗原表达的K562细胞能通过激活共刺激信号促进NK细胞的增殖,据报道,当K562细胞作为饲养细胞与IL-2和IL-15联合使用时,NK细胞的扩增超过300倍。

一些PBMC来源NK细胞的扩增方法
肿瘤细胞膜颗粒也是肿瘤细胞系扩增NK细胞的有效替代品,其不仅保持了诱导NK细胞扩增的膜受体的激活效率,而且避免了肿瘤细胞与扩增产物混合的风险。
新的无饲养层扩张系统正在开发中,细胞因子如IL-2、IL-15和IL-21的单一或简单组合被用于扩增细胞。细胞因子、链球菌和唑来膦酸盐刺激脐血单个核细胞3周,可产生平均纯度为95%的NK细胞,扩增倍数可达1561倍。这种无饲养层的方法降低了将其他类型的细胞引入最终产品的风险,但NK细胞的纯度仍需提高。
II.NK细胞系
NK-92是第一个获得FDA批准用于临床试验的基于NK细胞的细胞系,是一种同质的永生化NK淋巴瘤细胞系,可以在体外扩增以获得大量细胞。NK-92细胞表面标志CD56和CD25阳性,CD3、CD4、CD8、CD16、CD32、CD64和HLA-DR阴性。NK-92细胞的生长依赖于IL-2。由于其致癌特性,需要在患者给药之前对NK-92衍生细胞产品进行辐射,这反过来又对其在体内的长期持久性和整体治疗潜力产生负面影响。另一个缺点是,由于缺乏CD16的表达,NK-92细胞缺乏通过ADCC介导细胞杀伤的能力。
【CAR-NK的比较优势】
不同于T细胞,NK细胞的一大独特之处在于,并不局限于自体细胞,目前的临床研究显示CAR-NK细胞不会产生GvHD(移植物抗宿主病),因此安全性较高。同种异体CAR-NK获取方便,质量均一且时效高,副作用小。
【相关产品列表】
细胞分离
品牌 | 货号 | 产品名称 |
Seebio | ACJ0020A | Polysucrose 400 聚蔗糖400 |
血清
品牌 | 货号 | 产品名称 | 规格 |
Seebio | EEM0020D | 优级胎牛血清 | 500ml |
Seebio | EBM0084A | 小牛血清 | 100ml、500ml |
Seebio | DDJ0002B | 特级新生牛血清 | 100ml |
细胞因子
货号 | 产品名称 | 包装规格 |
EDQ0056A | 重组人 BMP-2(rhBMP-2) | 50ug、1mg |
EDQ0057A | 重组人 BMP-4(rhBMP-4) | 50ug、1mg |
EDQ0058A | 重组人 BMP-7(rhBMP-7) | 10ug、50ug、1mg |
EDQ0061A | 重组人表皮生长因子(rhEGF) | 10ug、50ug、1mg |
EDQ0083A | 重组人 Noggin(rhNoggin) | 50ug、1mg |
EDQ0086A | 重组人 R-spondin(rhR-spondin) | 50ug、1mg |
EDQ0092A | 重组人 Wnt-3α(rhWnt-3α) | 50ug、1mg |
EDQ0106A | 重组人白细胞介素-2(rhIL-2) | 100ug、1mg |
EDQ0112A | 重组人白细胞介素-15(rhIL-15) | 50ug、1mg |
EDQ0113A | 重组人白细胞介素-17(rhIL-17) | 50ug、1mg |
EDQ0115A | 重组人白细胞介素-21(rhIL-21) | 50ug、100μg、1mg |
EDQ0096A | 重组人粒细胞集落刺激因子(rhG-CSF) | 1mg |
EDQ0097A | 重组人粒细胞巨噬细胞刺激因子(rhGM-CSF) | 100ug、1mg |
细胞抗结团 & 表面活性剂 & 消泡剂
品牌 | 货号 | 产品名称 | 规格 |
Seebio | DCJ0018D | 硫酸葡聚糖 5000(DSS),低内毒素 | 1g、25g、100g、500g |
Seebio | DCJ1606D | Seebio® 硫酸葡聚糖钠盐 40,000(DSS),低内毒素 | 1g、25g、100g、500g |
Seebio | DCH0535A | Seebio® P188 非离子表面活性剂(100×) | 50ml |
Seebio | ACH0497B | 泊洛沙姆188(药用级) | 1kg、20kg |
Seebio | DGF6890 | 亚油酸钠 | 1kg、25kg |
Seebio | ABY0110A | 金精三羧酸铵盐 | 50g、100g、500g |
Seebio | ACH0558A | 有机硅消泡剂 | 25g、100g、500g |
Seebio | ACH0476A-500g | 非离子型T-F复合型发酵用消泡剂 | 500g |
ITS添加剂原料
品牌 | 货号 | 产品名称 | 规格 |
Seebio | EYY3311 | 重组人胰岛素 | 1g |
Seebio | DBM0012 | 转铁蛋白 | 100mg、500mg、1g |
Seebio | DCL0001 | 牛血清白蛋白 | 1g、5g、25g、1kg |
Seebio | AJL0068 | 丙酮酸钠 | 1kg、25kg |
Seebio | EDQ0163A | 胎球蛋白A(FetuinA) | 100mg |
Seebio | EDQ0165A | 纤连蛋白(Fibronectin) | 10ug、50ug |
细胞冻存
品牌 | 货号 | 产品名称 | 规格 |
Seebio | AJL0007A | 二甲基亚砜(DMSO) | 500ml,4L |
wako | 302-14686 | BAMBANKER冻存液 | 100 mL |
wako | 306-14684 | BAMBANKER冻存液 | 20 mLx5 |



