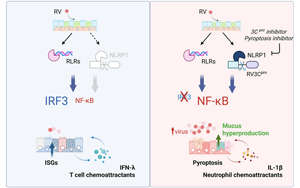
当引起普通感冒的最常见原因鼻病毒感染我们的鼻道内壁时,我们的细胞会通过触发抗病毒防御武器库来共同对抗病毒。在1月19日发表在Cell Press杂志《Cell Press Blue》上的一篇论文中,研究人员展示了我们鼻子里的细胞如何协同工作,保护我们免受普通感冒的侵害,并表明我们身体对鼻病毒的防御——而不是病毒本身——通常预测我们是否会感冒,以及我们的症状会有多严重。
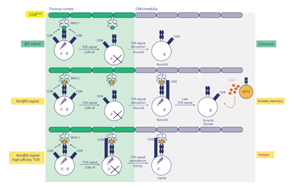
胸腺肽选择性决定CD8+T细胞功能亚群分化的新机制:β5t肽与非β5t肽通过调控TCR信号持续性引导谱系命运
为了深入探究MHC-I限制性CD8+T细胞的谱系命运决定机制,由Miho Shinzawa和Alfred Singer等人组成的研究团队在《Nature Immunology》上发表了他们的最新研究。他们设计了一个巧妙的遗传学模型——CD8Dual小鼠。这种小鼠的Cd4和Cd8基因座都编码CD8共受体蛋白,但分别产生略有差异的CD8.1(由Cd4基因座编码)和CD8.2(由Cd8基因座编码)共受体。这一设计使得研究人员能够剥离共受体蛋白本身的功能,而专注于研究编码这些共受体的基因座(Cd4 或 Cd8)对
Sevabertinib:一种可逆性HER2抑制剂在肺癌中的临床前活性与临床潜力
本文推荐一篇关于可逆性HER2抑制剂Sevabertinib(BAY 2927088)的研究。该研究通过临床前模型(包括携带HER2外显子20插入、点突变和扩增的肺癌模型)及早期临床试验数据,证实Sevabertinib可有效抑制HER2信号通路,并对NRG1融合模型也展示活性。
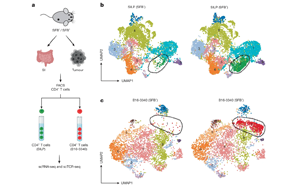
肠道菌群诱导的T细胞可塑性:微生物抗原模拟增强免疫检查点阻断疗效的新机制
研究发现,仅在同时存在SFB定植且肿瘤表达SFB抗原(B16-3340)并接受抗PD-1抗体治疗的小鼠中,肿瘤生长被显著抑制,而对照肿瘤(B16-EV)或无SFB定植的小鼠则无此效果。存活小鼠对再次接种的相同肿瘤细胞产生排斥,表明SFB与ICB联合可诱导持久的记忆样保护。此外,在肿瘤植入后不同时间点给予SFB的治疗性定植实验表明,早期微生物抗原暴露与PD-1阻断的协同作用窗口期较窄。
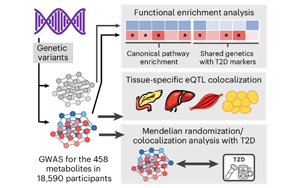
循环代谢物、遗传与生活方式因素在2型糖尿病未来风险中的综合作用研究
研究整合了十项队列中超过23,000人的血液代谢组、基因组和生活方式数据,系统鉴定出235种与2型糖尿病(T2D)风险相关的代谢物,揭示了遗传和可调控因素通过脂代谢、氨基酸、胆汁酸等通路影响T2D发病机制的分子基础,并构建了可提升风险预测精度的44代谢物标志物。
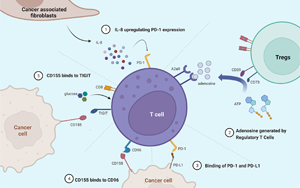
《自然免疫学》:对如何利用免疫系统对抗癌症有了新的认识
乔治城大学隆巴迪综合癌症中心的研究人员发现了一种重新编程 T 细胞(一种对抗感染和肿瘤的白细胞)的新方法,使其具有更强的记忆力,从而更有效地杀死癌细胞。该研究结果于 2026 年 1 月 12 日发表在《自然免疫学》杂志上,它强化了一种已知的策略,即阻断 PARP 的细胞活性。PARP 是一种能够检测细胞中 DNA 异常并进行修复的酶。
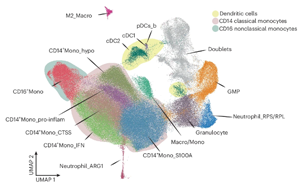
Nature Cancer:单细胞分析揭示多发性骨髓瘤的免疫景观
西奈山伊坎医学院、佐治亚理工学院和圣路易斯华盛顿大学等机构的科学家们近日构建了迄今为止规模最大的多发性骨髓瘤患者的骨髓单细胞免疫图谱。这项研究成果于1月9日发表在《Nature Cancer》杂志上,为了解骨髓瘤中的免疫功能障碍提供了前所未有的见解,并有望开发出更精准的工具来预测哪些患者在治疗后复发风险更高。
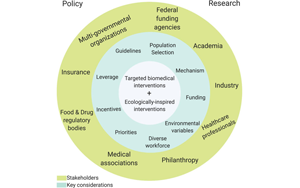
《PNAS》你的肠道微生物可能正在悄然改变你的大脑运作方式
一项新的研究表明,改变肠道内微生物群落可以影响大脑功能。人类是灵长类动物中脑容量与体型比例最大的,但科学家们仍然没有完全了解拥有更大脑容量的物种是如何进化出满足大脑发育和维持所需高能量消耗的方法的。西北大学的研究人员现在提供了第一个直接证据,证明肠道微生物群有助于塑造灵长类动物不同物种的大脑功能差异。
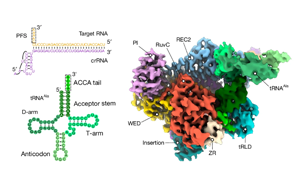
RNA触发的Cas12a3通过切割tRNA尾部执行细菌免疫新机制
CRISPR-Cas系统家族新成员——Cas12a3,其被靶RNA激活后可特异性切割tRNA的3′端CCA尾部,介导独特的抗噬菌体免疫反应。该研究通过生化和结构分析揭示了Cas12a3的tRNA装载域(tRLD)精准定位底物的机制,并开发了基于此特性的多重RNA检测新工具,为CRISPR工具箱拓展了全新方向。