摘要:科学家们通过系统性的CRISPR筛选,发现PTGES3竟然是雄激素受体的一个意想不到的调节因子。
一种此前特性不明的蛋白质,过去被认为是分子伴侣或酶,实际上可能在前列腺癌中扮演着关键角色。在一次系统的CRISPR筛选中,来自Arc研究所、加州大学旧金山分校和弗雷德·哈钦森癌症中心的科学家们发现,PTGES3(第三种前列腺素E合成酶)竟然是雄激素受体的一个意想不到的调节因子。这项发现于11月5日发表在《自然·遗传学》杂志上,不仅重新定义了PTGES3在基因表达调控中的生物学作用,还揭示了一个有望用于治疗对现有激素疗法耐药的侵袭性前列腺癌的新靶点。

图1 全基因组CRISPR筛选鉴定PTGES3为晚期前列腺癌中雄激素受体的直接调节因子
研究团队在开发出一种能够实时追踪雄激素受体水平的荧光标记后,发现了这种关联。雄激素受体是一种激素感应蛋白,通常有助于前列腺的发育和维持。在前列腺癌细胞中,雄激素受体活性显著增强,并驱动肿瘤的侵袭性进展,使其成为当前治疗的主要靶点。这项标记技术的创新使得科学家能够进行全基因组CRISPR筛选,从而识别出哪些基因对于维持侵袭性前列腺癌细胞中的雄激素受体水平至关重要。
在筛选过程中,研究人员逐一关闭基因,以观察哪些基因会导致发光的雄激素受体蛋白消失。筛选结果证实了已知的雄激素受体调节因子,例如 HOXB13 和 GATA2,验证了该方法的有效性,但也发现了一些意想不到的候选基因,例如 PTGES3。由于 PTGES3 是三种相关的合成前列腺素酶中唯一影响雄激素受体水平的酶,因此结果表明它可能并非之前认为的那样发挥作用。
“我们的研究展现了CRISPR技术在定量、无偏倚的蛋白质研究中的强大作用,它能帮助我们发现一些关于研究充分的蛋白质的新信息,”资深作者卢克·吉尔伯特(Luke Gilbert,@LukeGilbertSF)说道,他是Arc研究所的核心研究员,也是加州大学旧金山分校医学院泌尿外科副教授。“我们最初的目标是寻找可能调控雄激素受体生物学的酶,因为它们是药物靶点,但最终我们发现了PTGES3,一种据我们所知并非酶的蛋白质,它却对雄激素受体产生了深远的影响。”
为了进一步探究PTGES3在前列腺癌中的潜在作用,研究团队分析了患者数据,结果显示PTGES3高表达的患者在接受激素治疗后疗效显著较差。小鼠研究表明,抑制PTGES3可延缓肿瘤生长并降低肿瘤内雄激素受体水平,提示PTGES3可能成为治疗耐药性癌症的新靶点。
研究人员证实,在癌细胞中,PTGES3 实际上通过双重机制发挥作用:一方面,它作为辅助伴侣蛋白,帮助稳定细胞质中的雄激素受体蛋白;另一方面,它作为核内辅助因子,使雄激素受体能够与 DNA 结合并激活其靶基因。如果雄激素受体是前列腺癌进展的驱动因素,那么研究人员提供的证据表明,肿瘤生长可能受到 PTGES3 的辅助,甚至依赖于 PTGES3。
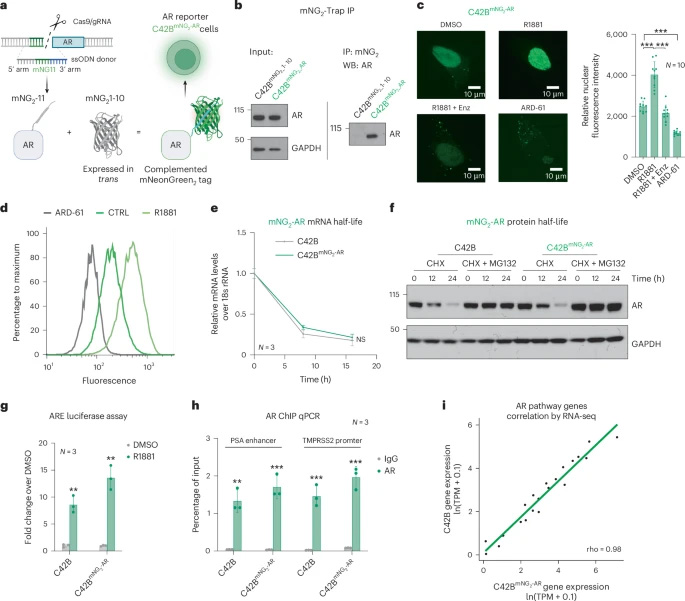
图2 在PCa细胞中建立内源性AR-mNG2荧光报告基因
“以往通过调控转录因子功能进行治疗的研究主要集中在DNA结合域和转录激活域。而针对转录因子稳定性调控因子的研究则相对较少,”该研究的第一作者李浩龙(音译)说道。他曾在加州大学旧金山分校(UCSF)开展这项研究,目前是弗雷德·哈钦森癌症研究中心(Fred Hutch)的助理教授。“我们的研究可以为理解不同激素驱动型癌症中其他重要的转录因子提供参考模板。未来,肿瘤学研究中至少有20种转录因子可以从这种方法中受益。”
研究团队目前正致力于了解PTGES3与雄激素受体相互作用的结构细节。他们的长期目标是开发针对这种相互作用的治疗方法,可能采用已在临床试验中展现出前景的蛋白质降解策略。
该研究的另一位资深作者,加州大学旧金山分校海伦·迪勒家族综合癌症中心放射肿瘤学、泌尿外科和内科学教授、转化研究副主任Felix Feng于去年12月去世。“我们深切缅怀费利克斯,并希望这项研究能成为他留下的宝贵遗产,”吉尔伯特说道。
参考资料
[1] Genome-scale CRISPR screens identify PTGES3 as a direct modulator of androgen receptor function in advanced prostate cancer
摘要:科学家们通过系统性的CRISPR筛选,发现PTGES3竟然是雄激素受体的一个意想不到的调节因子。
一种此前特性不明的蛋白质,过去被认为是分子伴侣或酶,实际上可能在前列腺癌中扮演着关键角色。在一次系统的CRISPR筛选中,来自Arc研究所、加州大学旧金山分校和弗雷德·哈钦森癌症中心的科学家们发现,PTGES3(第三种前列腺素E合成酶)竟然是雄激素受体的一个意想不到的调节因子。这项发现于11月5日发表在《自然·遗传学》杂志上,不仅重新定义了PTGES3在基因表达调控中的生物学作用,还揭示了一个有望用于治疗对现有激素疗法耐药的侵袭性前列腺癌的新靶点。

图1 全基因组CRISPR筛选鉴定PTGES3为晚期前列腺癌中雄激素受体的直接调节因子
研究团队在开发出一种能够实时追踪雄激素受体水平的荧光标记后,发现了这种关联。雄激素受体是一种激素感应蛋白,通常有助于前列腺的发育和维持。在前列腺癌细胞中,雄激素受体活性显著增强,并驱动肿瘤的侵袭性进展,使其成为当前治疗的主要靶点。这项标记技术的创新使得科学家能够进行全基因组CRISPR筛选,从而识别出哪些基因对于维持侵袭性前列腺癌细胞中的雄激素受体水平至关重要。
在筛选过程中,研究人员逐一关闭基因,以观察哪些基因会导致发光的雄激素受体蛋白消失。筛选结果证实了已知的雄激素受体调节因子,例如 HOXB13 和 GATA2,验证了该方法的有效性,但也发现了一些意想不到的候选基因,例如 PTGES3。由于 PTGES3 是三种相关的合成前列腺素酶中唯一影响雄激素受体水平的酶,因此结果表明它可能并非之前认为的那样发挥作用。
“我们的研究展现了CRISPR技术在定量、无偏倚的蛋白质研究中的强大作用,它能帮助我们发现一些关于研究充分的蛋白质的新信息,”资深作者卢克·吉尔伯特(Luke Gilbert,@LukeGilbertSF)说道,他是Arc研究所的核心研究员,也是加州大学旧金山分校医学院泌尿外科副教授。“我们最初的目标是寻找可能调控雄激素受体生物学的酶,因为它们是药物靶点,但最终我们发现了PTGES3,一种据我们所知并非酶的蛋白质,它却对雄激素受体产生了深远的影响。”
为了进一步探究PTGES3在前列腺癌中的潜在作用,研究团队分析了患者数据,结果显示PTGES3高表达的患者在接受激素治疗后疗效显著较差。小鼠研究表明,抑制PTGES3可延缓肿瘤生长并降低肿瘤内雄激素受体水平,提示PTGES3可能成为治疗耐药性癌症的新靶点。
研究人员证实,在癌细胞中,PTGES3 实际上通过双重机制发挥作用:一方面,它作为辅助伴侣蛋白,帮助稳定细胞质中的雄激素受体蛋白;另一方面,它作为核内辅助因子,使雄激素受体能够与 DNA 结合并激活其靶基因。如果雄激素受体是前列腺癌进展的驱动因素,那么研究人员提供的证据表明,肿瘤生长可能受到 PTGES3 的辅助,甚至依赖于 PTGES3。

图2 在PCa细胞中建立内源性AR-mNG2荧光报告基因
“以往通过调控转录因子功能进行治疗的研究主要集中在DNA结合域和转录激活域。而针对转录因子稳定性调控因子的研究则相对较少,”该研究的第一作者李浩龙(音译)说道。他曾在加州大学旧金山分校(UCSF)开展这项研究,目前是弗雷德·哈钦森癌症研究中心(Fred Hutch)的助理教授。“我们的研究可以为理解不同激素驱动型癌症中其他重要的转录因子提供参考模板。未来,肿瘤学研究中至少有20种转录因子可以从这种方法中受益。”
研究团队目前正致力于了解PTGES3与雄激素受体相互作用的结构细节。他们的长期目标是开发针对这种相互作用的治疗方法,可能采用已在临床试验中展现出前景的蛋白质降解策略。
该研究的另一位资深作者,加州大学旧金山分校海伦·迪勒家族综合癌症中心放射肿瘤学、泌尿外科和内科学教授、转化研究副主任Felix Feng于去年12月去世。“我们深切缅怀费利克斯,并希望这项研究能成为他留下的宝贵遗产,”吉尔伯特说道。
参考资料
[1] Genome-scale CRISPR screens identify PTGES3 as a direct modulator of androgen receptor function in advanced prostate cancer



