摘要:研究表明,MF59 佐剂 A(H5N8) 疫苗能够诱导强烈的免疫反应。
2023 年,芬兰爆发了影响野生鸟类和毛皮养殖场的大规模 2.3.4.4b 分支 A(H5N1) 疫情,芬兰成为第一个向高危职业群体提供 Seqirus 公司生产的 A(H5N8) 人畜共患禽流感疫苗的国家。
发表在《自然微生物学》上的一项新研究表明,MF59佐剂A(H5N8)疫苗能够诱导强烈的免疫反应,包括针对疫苗病毒的功能性抗体和记忆性T细胞反应,以及针对近期在欧洲和美国爆发的H5病毒的免疫反应。

图1 甲型H5N8流感疫苗可在高危人群中诱导针对高致病性禽流感分支2.3.4.4b甲型H5N1病毒的体液及细胞介导免疫反应
两剂后产生强烈的免疫反应
这项观察性 IV 期研究评估了 39 名高危个体的抗体反应和 18 名参与者子集中的 T 细胞反应。
接种两剂疫苗后,大多数先前未接种过疫苗的个体产生了针对疫苗病毒(A/Astrakhan/3212/2020,2.3.4.4b分支)的血清保护性抗体。通过微量中和试验(滴度≥20)测得的针对疫苗病毒的血清保护率为83%(95% CI 70–97%),通过血凝抑制试验(滴度≥40)测得的血清保护率为97%(90–100%)。
值得注意的是,这些抗体还能识别异源的2.3.4.4b分支H5毒株,包括在芬兰毛皮养殖场和美国奶牛养殖场暴发的H5N1病毒。
“这些研究结果表明,两剂疫苗可引发强烈的体液和细胞免疫反应,有望对目前流行的 2.3.4.4b 分支 H5 病毒提供保护,”作者报告说。
T 细胞分析进一步表明,在接种第二剂疫苗后,产生 IFN-γ 的 CD4? T 细胞数量增加了约五倍,这表明细胞免疫被激活,这可能有助于更广泛、更持久的保护。
单剂疫苗即可显著增强先前接种过疫苗者的免疫力。
其中一项最引人注目的发现与那些多年前甚至十多年前接种过H5疫苗的参与者有关。在这些个体中,单剂当前疫苗即可迅速诱导产生高水平的中和抗体,而间隔较短时间接种第二剂并未带来显著的额外增强效果。
这表明存在强大的免疫记忆,并提示即使流行的病毒与疫苗株不同,先用目前可用的疫苗对高危人群进行免疫,然后在未来的流行病期间进行加强免疫,也能提供快速而有效的保护。
高危人群疫苗接种率低
然而,芬兰的疫苗接种经验凸显了一个关键差距:根据国家疫苗接种登记数据,目标高风险人群的疫苗接种率远低于预期。在估计的目标职业类别中,只有不到10%的人接种了疫苗,而且并非所有人都完成了两剂接种。这强调了在未来的疫情防范工作中,需要改进沟通和参与策略。
尽管疫苗具有很强的免疫原性,但由于符合接种条件的人群参与率极低,其在现实世界中的应用受到限制。尤其值得注意的是,尽管开展了多项宣传活动,但没有一个毛皮养殖场工人参与这项研究,而他们是2023年疫情爆发期间暴露风险最高的群体。
其他符合条件的群体包括实验室人员、鸟类环志员、兽医和家禽养殖工人。实验室工作人员占免疫原性研究参与者的大多数。
疫苗接种率低的几个可能原因
在许多负责组织社会和医疗保健服务的福利服务县,疫苗的供应有限。一些人可能并不知道自己符合接种条件。他们可能对个人风险存在疑虑。由于疫苗上市前缺乏人体试验数据,有限的疫苗益处和安全性数据可能使人们对是否接种疫苗犹豫不决。
“即使疫苗具有很强的免疫原性,并且与流行的病毒非常匹配,它也只能保护那些接种疫苗的人,”作者强调说。
改进并制定更有针对性的沟通策略对于未来的疫苗接种活动至关重要。
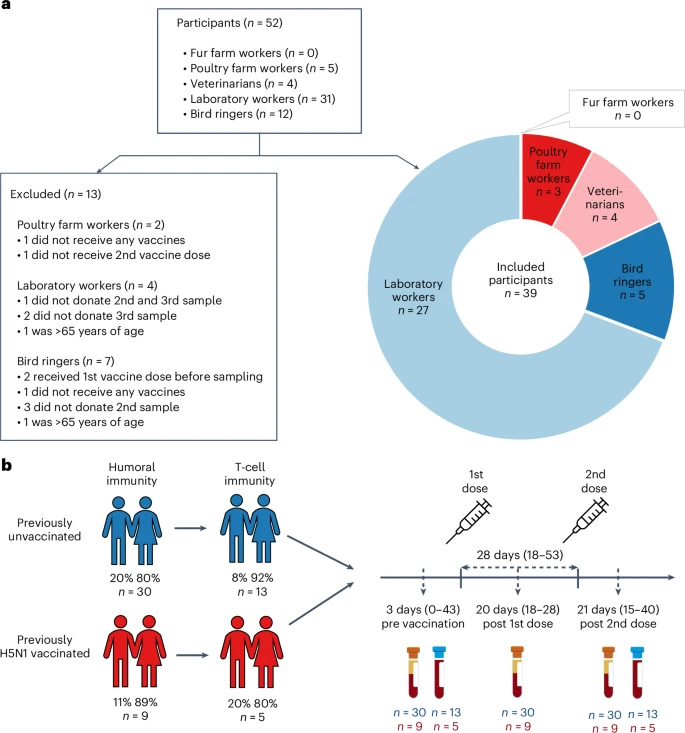
图2 研究概况
对全球禽流感防范的影响
各国正为H5N1禽流感在全球范围内可能出现的传播升级做准备,芬兰的经验为此提供了重要的指导。研究表明,两剂疫苗可在此前未接种过疫苗的人群中产生强烈的抗体和T细胞反应,而单剂疫苗则可在数年前甚至数十年前接种过任何H5疫苗的人群中迅速诱导产生高水平的免疫力。
这凸显了在疫情间歇期对高风险职业群体进行培训的重要性,以便在疫情恶化时能够迅速有效地加强对他们的防护。成功的准备工作还需要积极主动地与目标群体互动,以确保他们能够获得所需信息、提高意识并建立信任。
一项包括使用现有H5疫苗为高危人群进行初步免疫的策略既可持续又具有前瞻性。如果疫情迅速恶化,即使加强针的疫苗并非完全匹配,仍然可以提供及时有效的保护。
参考资料
[1] Influenza A(H5N8) vaccine induces humoral and cell-mediated immunity against highly pathogenic avian influenza clade 2.3.4.4b A(H5N1) viruses in at-risk individuals
摘要:研究表明,MF59 佐剂 A(H5N8) 疫苗能够诱导强烈的免疫反应。
2023 年,芬兰爆发了影响野生鸟类和毛皮养殖场的大规模 2.3.4.4b 分支 A(H5N1) 疫情,芬兰成为第一个向高危职业群体提供 Seqirus 公司生产的 A(H5N8) 人畜共患禽流感疫苗的国家。
发表在《自然微生物学》上的一项新研究表明,MF59佐剂A(H5N8)疫苗能够诱导强烈的免疫反应,包括针对疫苗病毒的功能性抗体和记忆性T细胞反应,以及针对近期在欧洲和美国爆发的H5病毒的免疫反应。

图1 甲型H5N8流感疫苗可在高危人群中诱导针对高致病性禽流感分支2.3.4.4b甲型H5N1病毒的体液及细胞介导免疫反应
两剂后产生强烈的免疫反应
这项观察性 IV 期研究评估了 39 名高危个体的抗体反应和 18 名参与者子集中的 T 细胞反应。
接种两剂疫苗后,大多数先前未接种过疫苗的个体产生了针对疫苗病毒(A/Astrakhan/3212/2020,2.3.4.4b分支)的血清保护性抗体。通过微量中和试验(滴度≥20)测得的针对疫苗病毒的血清保护率为83%(95% CI 70–97%),通过血凝抑制试验(滴度≥40)测得的血清保护率为97%(90–100%)。
值得注意的是,这些抗体还能识别异源的2.3.4.4b分支H5毒株,包括在芬兰毛皮养殖场和美国奶牛养殖场暴发的H5N1病毒。
“这些研究结果表明,两剂疫苗可引发强烈的体液和细胞免疫反应,有望对目前流行的 2.3.4.4b 分支 H5 病毒提供保护,”作者报告说。
T 细胞分析进一步表明,在接种第二剂疫苗后,产生 IFN-γ 的 CD4? T 细胞数量增加了约五倍,这表明细胞免疫被激活,这可能有助于更广泛、更持久的保护。
单剂疫苗即可显著增强先前接种过疫苗者的免疫力。
其中一项最引人注目的发现与那些多年前甚至十多年前接种过H5疫苗的参与者有关。在这些个体中,单剂当前疫苗即可迅速诱导产生高水平的中和抗体,而间隔较短时间接种第二剂并未带来显著的额外增强效果。
这表明存在强大的免疫记忆,并提示即使流行的病毒与疫苗株不同,先用目前可用的疫苗对高危人群进行免疫,然后在未来的流行病期间进行加强免疫,也能提供快速而有效的保护。
高危人群疫苗接种率低
然而,芬兰的疫苗接种经验凸显了一个关键差距:根据国家疫苗接种登记数据,目标高风险人群的疫苗接种率远低于预期。在估计的目标职业类别中,只有不到10%的人接种了疫苗,而且并非所有人都完成了两剂接种。这强调了在未来的疫情防范工作中,需要改进沟通和参与策略。
尽管疫苗具有很强的免疫原性,但由于符合接种条件的人群参与率极低,其在现实世界中的应用受到限制。尤其值得注意的是,尽管开展了多项宣传活动,但没有一个毛皮养殖场工人参与这项研究,而他们是2023年疫情爆发期间暴露风险最高的群体。
其他符合条件的群体包括实验室人员、鸟类环志员、兽医和家禽养殖工人。实验室工作人员占免疫原性研究参与者的大多数。
疫苗接种率低的几个可能原因
在许多负责组织社会和医疗保健服务的福利服务县,疫苗的供应有限。一些人可能并不知道自己符合接种条件。他们可能对个人风险存在疑虑。由于疫苗上市前缺乏人体试验数据,有限的疫苗益处和安全性数据可能使人们对是否接种疫苗犹豫不决。
“即使疫苗具有很强的免疫原性,并且与流行的病毒非常匹配,它也只能保护那些接种疫苗的人,”作者强调说。
改进并制定更有针对性的沟通策略对于未来的疫苗接种活动至关重要。

图2 研究概况
对全球禽流感防范的影响
各国正为H5N1禽流感在全球范围内可能出现的传播升级做准备,芬兰的经验为此提供了重要的指导。研究表明,两剂疫苗可在此前未接种过疫苗的人群中产生强烈的抗体和T细胞反应,而单剂疫苗则可在数年前甚至数十年前接种过任何H5疫苗的人群中迅速诱导产生高水平的免疫力。
这凸显了在疫情间歇期对高风险职业群体进行培训的重要性,以便在疫情恶化时能够迅速有效地加强对他们的防护。成功的准备工作还需要积极主动地与目标群体互动,以确保他们能够获得所需信息、提高意识并建立信任。
一项包括使用现有H5疫苗为高危人群进行初步免疫的策略既可持续又具有前瞻性。如果疫情迅速恶化,即使加强针的疫苗并非完全匹配,仍然可以提供及时有效的保护。
参考资料
[1] Influenza A(H5N8) vaccine induces humoral and cell-mediated immunity against highly pathogenic avian influenza clade 2.3.4.4b A(H5N1) viruses in at-risk individuals



