摘要:科学家在对抗导致人类疾病和流行病的RNA病毒方面取得了重要突破。
来自A*STAR新加坡基因组研究所(GIS)和新加坡国立大学医学院(NUS Medicine)的一组科学家在对抗导致人类疾病和流行病的RNA病毒方面取得了重要突破。
他们的研究表明,在实验室模型中,由腺相关病毒(AAV)传递的CRISPR-Cas13编辑器可以直接靶向并消除RNA病毒。AAV是由自然感染人类的小病毒衍生的运载工具。它们被临床批准用于基因治疗药物,用于治疗脊髓性肌萎缩症、杜氏肌营养不良症和血友病等疾病。

图1 科学家在对抗导致人类疾病和流行病的RNA病毒方面取得了重要突破
EV-A71病毒是导致手足口病的原因,在严重的情况下,可导致神经系统疾病和死亡。为了治疗病毒感染,研究小组求助于CRISPR-Cas13,这是一种RNA编辑技术,可以改变细胞中的RNA。
CRISPR-Cas13编辑RNA,为诺贝尔奖得主CRISPR-Cas9无法治疗的广泛疾病开辟了治疗途径,CRISPR-Cas9编辑DNA。CRISPR-Cas13是由引导RNA (grna)编程以靶向特定的RNA序列。在与这些RNA序列结合后,CRISPR-Cas13将RNA靶标切割成碎片,使RNA失活。CRISPR-Cas13还可以用于RNA编辑,将细胞内的特定RNA序列更改为另一个序列。
在最近的这项工作中,科学家团队首先开发了Cas13gRNAtor计算程序来设计CRISPR grna,这些grna可以切割不同病毒株的病毒RNA。他们表明,CRISPR-Cas13治疗有效地减少了病毒负担,只有不到0.1%的病毒留在先前感染的细胞中。
重要的是,研究结果表明,AAV-CRISPR-Cas13疗法可以清除EV-A71感染,防止器官损伤和死亡。
“这是一个惊人的证明,一剂CRISPR-Cas13可能意味着生与死的区别。我们正在以这项研究为基础,进一步开发改变生活的核酸疗法。A*STAR地理信息系统副主任兼首席科学家周伟梁博士说。
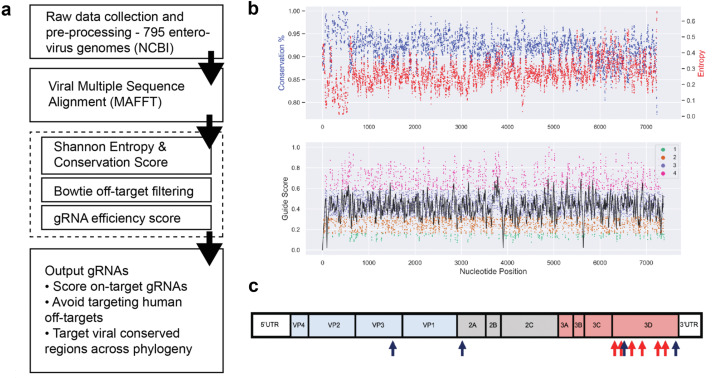
图2 CRISPR-CasRx-gRNA设计策略在细胞中产生具有强效和特异性抗病毒活性的gRNA
新加坡国立大学医学院微生物学、免疫学和传染病转化研究项目副教授Justin Chu补充说:“这项令人惊叹的研究通过使用AAV-CRISPR-Cas13对抗人类肠道病毒,帮助开辟了抗病毒策略的新领域,为潜在的病毒性疾病治疗铺平了道路。”
A*STAR地理信息系统代理执行主任刘建军教授说:“CRISPR技术允许重写几乎任何生物体的遗传密码。这项与新加坡国立大学的联合研究是一项极其重要的进展,它有可能治疗由RNA病毒引起的许多疾病,并为进一步的治疗方案开辟了许多途径。”
这些发现证明了抗病毒AAV-CRISPR-Cas13治疗潜在致命RNA病毒感染的开发管道。进一步的治疗发展可能会使这项技术用于临床治疗人类RNA病毒。这项研究于2023年6月28日发表在《电子生物医学》杂志上。
参考资料:
[1] AAV-CRISPR-Cas13 eliminates human enterovirus and prevents death of infected mice.
摘要:科学家在对抗导致人类疾病和流行病的RNA病毒方面取得了重要突破。
来自A*STAR新加坡基因组研究所(GIS)和新加坡国立大学医学院(NUS Medicine)的一组科学家在对抗导致人类疾病和流行病的RNA病毒方面取得了重要突破。
他们的研究表明,在实验室模型中,由腺相关病毒(AAV)传递的CRISPR-Cas13编辑器可以直接靶向并消除RNA病毒。AAV是由自然感染人类的小病毒衍生的运载工具。它们被临床批准用于基因治疗药物,用于治疗脊髓性肌萎缩症、杜氏肌营养不良症和血友病等疾病。

图1 科学家在对抗导致人类疾病和流行病的RNA病毒方面取得了重要突破
EV-A71病毒是导致手足口病的原因,在严重的情况下,可导致神经系统疾病和死亡。为了治疗病毒感染,研究小组求助于CRISPR-Cas13,这是一种RNA编辑技术,可以改变细胞中的RNA。
CRISPR-Cas13编辑RNA,为诺贝尔奖得主CRISPR-Cas9无法治疗的广泛疾病开辟了治疗途径,CRISPR-Cas9编辑DNA。CRISPR-Cas13是由引导RNA (grna)编程以靶向特定的RNA序列。在与这些RNA序列结合后,CRISPR-Cas13将RNA靶标切割成碎片,使RNA失活。CRISPR-Cas13还可以用于RNA编辑,将细胞内的特定RNA序列更改为另一个序列。
在最近的这项工作中,科学家团队首先开发了Cas13gRNAtor计算程序来设计CRISPR grna,这些grna可以切割不同病毒株的病毒RNA。他们表明,CRISPR-Cas13治疗有效地减少了病毒负担,只有不到0.1%的病毒留在先前感染的细胞中。
重要的是,研究结果表明,AAV-CRISPR-Cas13疗法可以清除EV-A71感染,防止器官损伤和死亡。
“这是一个惊人的证明,一剂CRISPR-Cas13可能意味着生与死的区别。我们正在以这项研究为基础,进一步开发改变生活的核酸疗法。A*STAR地理信息系统副主任兼首席科学家周伟梁博士说。

图2 CRISPR-CasRx-gRNA设计策略在细胞中产生具有强效和特异性抗病毒活性的gRNA
新加坡国立大学医学院微生物学、免疫学和传染病转化研究项目副教授Justin Chu补充说:“这项令人惊叹的研究通过使用AAV-CRISPR-Cas13对抗人类肠道病毒,帮助开辟了抗病毒策略的新领域,为潜在的病毒性疾病治疗铺平了道路。”
A*STAR地理信息系统代理执行主任刘建军教授说:“CRISPR技术允许重写几乎任何生物体的遗传密码。这项与新加坡国立大学的联合研究是一项极其重要的进展,它有可能治疗由RNA病毒引起的许多疾病,并为进一步的治疗方案开辟了许多途径。”
这些发现证明了抗病毒AAV-CRISPR-Cas13治疗潜在致命RNA病毒感染的开发管道。进一步的治疗发展可能会使这项技术用于临床治疗人类RNA病毒。这项研究于2023年6月28日发表在《电子生物医学》杂志上。
参考资料:
[1] AAV-CRISPR-Cas13 eliminates human enterovirus and prevents death of infected mice.



