摘要:格拉茨工业大学的研究人员对细菌中发现的一种蛋白质的功能有了新的认识,这种蛋白质的酶活性被蓝光激活。
光以许多不同的方式影响生物体:例如,植物的生长方向朝向太阳,而人类的昼夜节律是由日光控制的。这些过程总是涉及光感受器,光感受器是一种能感知不同颜色和光强度的蛋白质。
酶活性增加了一万倍
现在,格拉茨科技大学(TU Graz)的研究人员已经破译了一种高效光感受器的功能。他们的研究结果发表在《科学进展》杂志上。研究小组研究了一种在许多细菌中发现的二胍酸环化酶蛋白。它的酶功能调节了一种控制细菌生存方式的中心信使物质的产生。在黑暗中,这种蛋白质几乎完全不活跃,但一旦暴露在日光的蓝色成分中,它的酶活性就会迅速增加。格拉茨工业大学生物化学研究所光生化工作组负责人安德里亚斯·温克勒说:“这种蛋白质在光照下的酶活性比在黑暗中高出约1万倍。”在大多数光感受器中,活性增加了5到50倍,导致蛋白质活性的变化更加缓慢。Winkler解释说:“相比之下,我们所描述的蛋白质反应非常强烈,所以它实际上就像一个开关。”像这样的高效蛋白质开关可以在未来用于增强和优化光遗传学工具。

图1 研究发现二胍酸环化酶蛋白调节了一种控制细菌生存方式的中心信使物质的产生
蛋白质在蓝光下伸展
研究人员现在已经解开了蛋白质开关的结构和功能。这种蛋白质由两个功能部分组成:一个负责感知蓝光,另一个负责实际的酶活性,作为化学反应的催化剂。如果它暴露在蓝光下,蛋白质会改变其结构。当它不活跃时,整个蛋白质处于致密状态,但当它接触到光时,蛋白质拉伸,连接先前分离的酶部分。然后,这种蛋白质产生特定的信使分子,向细菌发出环境条件正在发生变化的信号。如果可能的话,细菌会适应这些新的环境。Andreas Winkler解释说:“这方面的一个例子是聚集体的形成,被称为生物膜,它使细菌更能抵抗环境的影响。”
潜在的医疗应用
“我真的很兴奋,我们的研究为这种迷人的蛋白质的机制提供了有价值的见解,”该研究的第一作者、格拉茨工业大学生物化学研究所的博士生Urula Vide评论道。“了解这种光激活酶开关背后的机制,为在一系列不同学科中的可能应用打开了大门。”其中之一是医学上使用的光基因治疗方法。与光调节蛋白开关相关的药物可以在精确的时间内仅在身体的一个非常有限的区域起作用,这将减少潜在的副作用。光诱导的蛋白质开关也将为细胞生物学的研究带来好处,因为它可以在分子水平上有针对性地触发特定的变化,然后可以更有效地分析这些变化。“但是我们离这种特殊开关的实际应用还有很长的路要走,”Winkler指出。然而,他相信他的团队的研究已经产生了一些重要的、基本的见解。
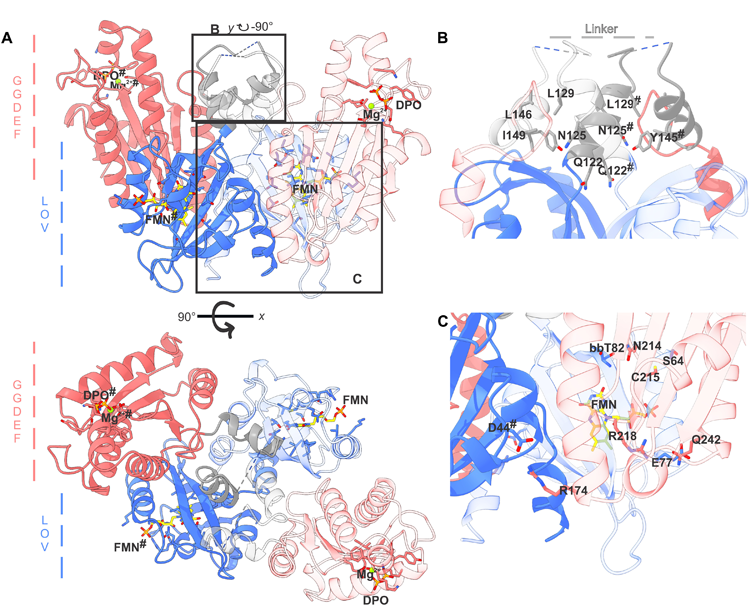
图2 MsLadC二聚体在其暗适应状态下的晶体结构
三维模型
在他们的实验中,研究人员没有从原始细菌中分离出蛋白质,而是在基因工程的帮助下在实验室中制造出蛋白质。他们用x射线衍射分析了分子结构,这是三维模型的基础。结合补充实验,该模型使研究人员能够推断出暴露在蓝光下蛋白质结构的变化,从而转化为关于生物开关分子功能的具体结论。
参考资料:
[1] Illuminating the inner workings of a natural protein switch: Blue-light sensing in LOV-activated diguanylate cyclases
摘要:格拉茨工业大学的研究人员对细菌中发现的一种蛋白质的功能有了新的认识,这种蛋白质的酶活性被蓝光激活。
光以许多不同的方式影响生物体:例如,植物的生长方向朝向太阳,而人类的昼夜节律是由日光控制的。这些过程总是涉及光感受器,光感受器是一种能感知不同颜色和光强度的蛋白质。
酶活性增加了一万倍
现在,格拉茨科技大学(TU Graz)的研究人员已经破译了一种高效光感受器的功能。他们的研究结果发表在《科学进展》杂志上。研究小组研究了一种在许多细菌中发现的二胍酸环化酶蛋白。它的酶功能调节了一种控制细菌生存方式的中心信使物质的产生。在黑暗中,这种蛋白质几乎完全不活跃,但一旦暴露在日光的蓝色成分中,它的酶活性就会迅速增加。格拉茨工业大学生物化学研究所光生化工作组负责人安德里亚斯·温克勒说:“这种蛋白质在光照下的酶活性比在黑暗中高出约1万倍。”在大多数光感受器中,活性增加了5到50倍,导致蛋白质活性的变化更加缓慢。Winkler解释说:“相比之下,我们所描述的蛋白质反应非常强烈,所以它实际上就像一个开关。”像这样的高效蛋白质开关可以在未来用于增强和优化光遗传学工具。

图1 研究发现二胍酸环化酶蛋白调节了一种控制细菌生存方式的中心信使物质的产生
蛋白质在蓝光下伸展
研究人员现在已经解开了蛋白质开关的结构和功能。这种蛋白质由两个功能部分组成:一个负责感知蓝光,另一个负责实际的酶活性,作为化学反应的催化剂。如果它暴露在蓝光下,蛋白质会改变其结构。当它不活跃时,整个蛋白质处于致密状态,但当它接触到光时,蛋白质拉伸,连接先前分离的酶部分。然后,这种蛋白质产生特定的信使分子,向细菌发出环境条件正在发生变化的信号。如果可能的话,细菌会适应这些新的环境。Andreas Winkler解释说:“这方面的一个例子是聚集体的形成,被称为生物膜,它使细菌更能抵抗环境的影响。”
潜在的医疗应用
“我真的很兴奋,我们的研究为这种迷人的蛋白质的机制提供了有价值的见解,”该研究的第一作者、格拉茨工业大学生物化学研究所的博士生Urula Vide评论道。“了解这种光激活酶开关背后的机制,为在一系列不同学科中的可能应用打开了大门。”其中之一是医学上使用的光基因治疗方法。与光调节蛋白开关相关的药物可以在精确的时间内仅在身体的一个非常有限的区域起作用,这将减少潜在的副作用。光诱导的蛋白质开关也将为细胞生物学的研究带来好处,因为它可以在分子水平上有针对性地触发特定的变化,然后可以更有效地分析这些变化。“但是我们离这种特殊开关的实际应用还有很长的路要走,”Winkler指出。然而,他相信他的团队的研究已经产生了一些重要的、基本的见解。

图2 MsLadC二聚体在其暗适应状态下的晶体结构
三维模型
在他们的实验中,研究人员没有从原始细菌中分离出蛋白质,而是在基因工程的帮助下在实验室中制造出蛋白质。他们用x射线衍射分析了分子结构,这是三维模型的基础。结合补充实验,该模型使研究人员能够推断出暴露在蓝光下蛋白质结构的变化,从而转化为关于生物开关分子功能的具体结论。
参考资料:
[1] Illuminating the inner workings of a natural protein switch: Blue-light sensing in LOV-activated diguanylate cyclases



