摘要:丹麦奥胡斯大学的研究人员近日利用CRISPR-Cas9系统开发出一种基因疗法,可以阻止这种侵袭性AML亚型的细胞分裂
急性髓系白血病(AML)是成年人最常见的急性白血病,其特点是大量异常分化的髓系细胞发生不可控制的增殖。部分癌症是由细胞分裂过程中的不同基因融合引起的。这种融合导致细胞生长不受控制。
丹麦奥胡斯大学的研究人员近日利用CRISPR-Cas9系统开发出一种基因疗法,可以阻止这种侵袭性AML亚型的细胞分裂,为AML的治疗提供了一种很有前景的治疗方法。
这项研究成果于近日发表在《Leukemia》杂志上。尽管这项研究的重点是血液癌症,但其他许多类型的癌症也是由融合基因驱动的,如部分肺癌和肉瘤。故研究人员推测,这项技术可以成为一种平台技术,用于治疗由基因融合驱动的特定癌症类型。

图1 利用CRISPR-Cas9系统开发出一种基因疗法
简单地说,研究人员成功地打断了驱动癌症的融合基因,这些基因错误地融合在一起,并向细胞发送致命信号,使细胞开始不受控制地分裂。当融合基因被打断时,癌细胞就会停止分裂。到目前为止,他们已在细胞系和小鼠身上试验了这种基因疗法。
在实验室环境下,他们采用电穿孔的方式将Cas9酶和向导RNA导入细胞。“你可以在实验室中使用这种方法,但不能在患者身上使用。我们需要研究如何将Cas9酶和向导RNA同时送入癌细胞,”奥胡斯大学临床医学系副教授Maja Ludvigsen说。
他补充说,作者们已经在一项平行研究中使用脂肪颗粒作为递送载体。作为COVID-19的mRNA疫苗的递送策略,这种方法非常有效。
研究人员将带有基因融合的癌细胞植入小鼠的两侧。未经处理的细胞系长成了巨大的肿瘤,而细胞经过处理后,也就是在植入小鼠体内之前接受过基因治疗,肿瘤要小得多,或者根本没有肿瘤。
“我们的基因疗法在实验室中似乎非常有效。我们不知道这种疗法是否足够有效,可应对所有的癌细胞。但在癌症研究领域有一个假设,如果一种治疗方法能够靶向大多数癌细胞,那么剩下的就交给免疫系统,” Maja Ludvigsen说。
研究人员的下一个任务是证明采用最佳递送策略的治疗方法也适用于带有特定基因融合的白血病小鼠。
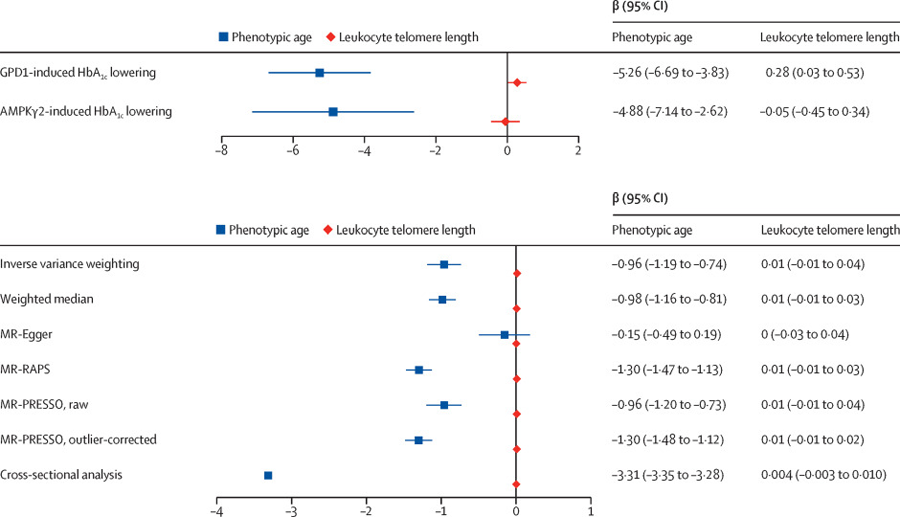
双内含子靶向CRISPR-Cas9介导RUNX1-RUNX1T1的破坏
他们还将研究这种治疗策略对于其他的融合驱动型癌症来说是否是一种更好的治疗选择。不过他们仍有一段路要走。例如,研究人员还不知道这种基因疗法的潜在副作用。
“挑战之一在于,如果我们能够在癌细胞中切割DNA,那么我们也会在其他健康细胞中切割相同的染色体。由于融合基因不存在于健康细胞中,我们的理论是健康细胞可以自己修复DNA,不过,我们必须对此进行更深入的研究,”Maja Ludvigsen解释说。
这项研究成果代表了人们朝着了解和治疗融合驱动型癌症迈出了重要一步。“虽然仍然处于转化研究阶段,但这是一个突破,因为我们已经成功地使用CRISPR/Cas9技术对驱动癌症的特定融合基因进行靶向治疗,”Maja Ludvigsen说,他希望五年内可以开始临床试验。
“尽管未来还有很多工作要做,但这一结果给那些机会有限的患者带来了治疗的希望。未来,我希望我们能够推出一种更温和、更有效且没有严重副作用的治疗方法,”Maja Ludvigsen说。
参考资料:
[1] Neldeborg, S., Soerensen, J.F., Møller, C.T. et al. Dual intron-targeted CRISPR-Cas9-mediated disruption of the AML RUNX1-RUNX1T1 fusion gene effectively inhibits proliferation and decreases tumor volume in vitro and in vivo. Leukemia (2023). https://doi.org/10.1038/s41375-023-01950-9
摘要:丹麦奥胡斯大学的研究人员近日利用CRISPR-Cas9系统开发出一种基因疗法,可以阻止这种侵袭性AML亚型的细胞分裂
急性髓系白血病(AML)是成年人最常见的急性白血病,其特点是大量异常分化的髓系细胞发生不可控制的增殖。部分癌症是由细胞分裂过程中的不同基因融合引起的。这种融合导致细胞生长不受控制。
丹麦奥胡斯大学的研究人员近日利用CRISPR-Cas9系统开发出一种基因疗法,可以阻止这种侵袭性AML亚型的细胞分裂,为AML的治疗提供了一种很有前景的治疗方法。
这项研究成果于近日发表在《Leukemia》杂志上。尽管这项研究的重点是血液癌症,但其他许多类型的癌症也是由融合基因驱动的,如部分肺癌和肉瘤。故研究人员推测,这项技术可以成为一种平台技术,用于治疗由基因融合驱动的特定癌症类型。

图1 利用CRISPR-Cas9系统开发出一种基因疗法
简单地说,研究人员成功地打断了驱动癌症的融合基因,这些基因错误地融合在一起,并向细胞发送致命信号,使细胞开始不受控制地分裂。当融合基因被打断时,癌细胞就会停止分裂。到目前为止,他们已在细胞系和小鼠身上试验了这种基因疗法。
在实验室环境下,他们采用电穿孔的方式将Cas9酶和向导RNA导入细胞。“你可以在实验室中使用这种方法,但不能在患者身上使用。我们需要研究如何将Cas9酶和向导RNA同时送入癌细胞,”奥胡斯大学临床医学系副教授Maja Ludvigsen说。
他补充说,作者们已经在一项平行研究中使用脂肪颗粒作为递送载体。作为COVID-19的mRNA疫苗的递送策略,这种方法非常有效。
研究人员将带有基因融合的癌细胞植入小鼠的两侧。未经处理的细胞系长成了巨大的肿瘤,而细胞经过处理后,也就是在植入小鼠体内之前接受过基因治疗,肿瘤要小得多,或者根本没有肿瘤。
“我们的基因疗法在实验室中似乎非常有效。我们不知道这种疗法是否足够有效,可应对所有的癌细胞。但在癌症研究领域有一个假设,如果一种治疗方法能够靶向大多数癌细胞,那么剩下的就交给免疫系统,” Maja Ludvigsen说。
研究人员的下一个任务是证明采用最佳递送策略的治疗方法也适用于带有特定基因融合的白血病小鼠。

双内含子靶向CRISPR-Cas9介导RUNX1-RUNX1T1的破坏
他们还将研究这种治疗策略对于其他的融合驱动型癌症来说是否是一种更好的治疗选择。不过他们仍有一段路要走。例如,研究人员还不知道这种基因疗法的潜在副作用。
“挑战之一在于,如果我们能够在癌细胞中切割DNA,那么我们也会在其他健康细胞中切割相同的染色体。由于融合基因不存在于健康细胞中,我们的理论是健康细胞可以自己修复DNA,不过,我们必须对此进行更深入的研究,”Maja Ludvigsen解释说。
这项研究成果代表了人们朝着了解和治疗融合驱动型癌症迈出了重要一步。“虽然仍然处于转化研究阶段,但这是一个突破,因为我们已经成功地使用CRISPR/Cas9技术对驱动癌症的特定融合基因进行靶向治疗,”Maja Ludvigsen说,他希望五年内可以开始临床试验。
“尽管未来还有很多工作要做,但这一结果给那些机会有限的患者带来了治疗的希望。未来,我希望我们能够推出一种更温和、更有效且没有严重副作用的治疗方法,”Maja Ludvigsen说。
参考资料:
[1] Neldeborg, S., Soerensen, J.F., Møller, C.T. et al. Dual intron-targeted CRISPR-Cas9-mediated disruption of the AML RUNX1-RUNX1T1 fusion gene effectively inhibits proliferation and decreases tumor volume in vitro and in vivo. Leukemia (2023). https://doi.org/10.1038/s41375-023-01950-9



