摘要:T细胞有一种核受体,它的作用非常奇怪——但非常重要——帮助T细胞对抗病原体和摧毁癌细胞。
根据发表在《Immunity》杂志上的一项新研究,T细胞有一种核受体,它的作用非常奇怪——但非常重要——帮助T细胞对抗病原体和摧毁癌细胞。这种受体被称为视黄酸受体α (RARα),已知控制细胞核内的基因表达程序,但它现在似乎也在细胞核外运作,协调细胞表面触发的导致T细胞活化的早期事件。

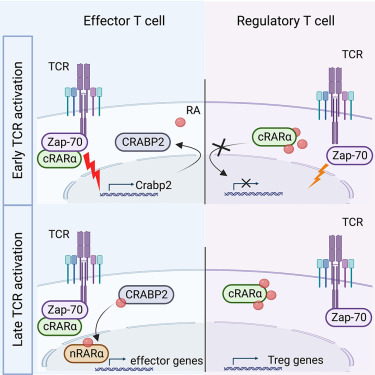
图1 视黄酸受体α (RARα)帮助T细胞对抗病原体和摧毁癌细胞
科学家们通常不会期望看到像RARα这样的核受体在细胞核外发挥这种作用。然而,新的发现表明,如果细胞质中没有一种形式的RARα, T细胞就无法开始对抗疾病。
“细胞质视黄酸受体是T细胞连接细胞表面感应与下游信号级联和基因表达程序的中心,将T细胞转化为活跃的战斗机,”Hilde Cheroutre教授说。
这项研究也是日本理研综合医学科学中心的科学家、加州大学圣地亚哥分校和索尔克研究所的当地团队成功合作的结果。
帮助T细胞应对危险
为了理解这一发现,它有助于描绘T细胞的地理位置。细胞核(与其捆绑的DNA)位于细胞的中间。被称为细胞器的其他分子和细胞结构漂浮在细胞核外的细胞质中,细胞质被细胞边缘的膜(细胞膜)包围。
被称为T细胞受体(TCRs)的特殊分子位于细胞膜上,在那里它们接收来自其他细胞的信息。你可以把TCRs想象成火灾观测者,从荒野中遥远的小木屋中扫描烟雾的瞭望者。就像火灾侦察员需要提醒官员注意远处的烟雾一样,如果TCRs检测到潜在的威胁,比如病毒或癌细胞,它们需要迅速向总部——细胞核发出信号。
将信号发送到细胞核对于激活基因表达将T细胞转化为战斗细胞至关重要。但TCRs不能只是接电话,那么它们是如何提醒远处的细胞核有麻烦的呢?
信号传递的过程令人着迷。一旦TCR被触发,被称为激酶的分子(将磷酸盐添加到蛋白质上的酶)与接头一起工作,接头告诉附近的蛋白质“点击”在一起,并组装一个特殊的分子“激活复合物”。这种复合物被称为TCR信号体,它在细胞膜内聚集。Cheroutre说:“TCR信号体对于调解细胞内外之间的通信非常重要。”
虽然TCR信号体已经被许多人研究了许多年,但在此之前还没有人在这个激活复合体中检测到RARα。
“这个新发现将改变我们对TCR信号的看法,”Kronenberg说。
揭示RARα的作用
RARα的秘密得以曝光,要归功于CRISPR技术的发展、成像和质谱技术的进步,以及LJI团队和合作者多年来的辛勤工作。
RARα属于视黄酸受体大家族,通常位于细胞核靶基因的控制区域。这些视黄酸受体招募抑制因子和激活因子分子,让它们“关闭”或“打开”这些靶基因的表达。视黄酸受体在细胞核中的这一重要作用为其赢得了“核受体”的称号。
几年前,Cheroutre和她的同事发表了一项研究,表明我们从维生素A中获得的视黄酸(RA)触发核RARα和基因表达,这对抑制调节性T细胞的分化很重要,从而降低免疫反应。
在这项新的研究中,Cheroutre想要研究维甲酸是如何控制这种抑制性T细胞的命运的,所以她的实验室开始更密切地研究维甲酸受体,比如RARα。
研究人员很感兴趣地发现RARα实际上有两种变体,称为同种异构体。“这些同工异构体由相同的基因编码,但它们在一端有一点不同。然而,其结果更为显著,将一种形式锁定在细胞质中,而另一种形式则被限制在细胞核中。”
这两种亚型在T细胞中扮演不同的角色吗?仔细观察后,研究人员意识到这种RARα异构体对维甲酸没有反应,甚至没有合适的设备来充当核受体。
“它没有对核受体很重要的工具,即与DNA相互作用的能力,以及从细胞质转移到细胞核的能力,”Cheroutre说。
利用CRISPR基因编辑技术调节这两种异构体的表达,研究人员发现,调节细胞质异构体会对细胞质中的TCR信号传导造成重大问题,并损害与细胞核控制中心的通信。
RARα在正确的时间出现在正确的位置
一旦他们知道在哪里寻找RARα同种异构体,研究人员就试图找出RARα与其他蛋白质的相互作用。这项工作揭示了与激酶ZAP70的相互作用,ZAP70是TCR信号体的主要成分。
另一个重要的早期线索是,RARα在细胞核外发挥作用,来自Myers实验室领导的蛋白质组学研究。研究人员使用质谱技术检测磷酸化过程,这是一个称为磷酸化基团的分子通过上游激酶附着在蛋白质上的过程。
对T细胞来说,当威胁临近时,磷酸化会刺激关键蛋白发挥作用。“在T细胞刺激的第一个小时左右,会发生成百上千个动态磷酸化事件,”Myers说。
当Myers和他的同事检查他们的数据时,他们惊讶地发现了与RARα相关的磷酸化事件。事实上,RARα的磷酸化在T细胞激活3分钟后就开始了。Myers说:“因为这个事件发生得很早,我们的发现表明RARα的磷酸化在T细胞受体附近,在TCR受到刺激后,它的活性就会爆发。”
这一发现进一步证明RARα的细胞质同工型是由TCR激活的,而不是像核RARα那样由RA激活。因此,这种新形式的RARα代表了细胞表面TCR/ZAP70激活复合物的重要组成部分。
然后,Cheroutre和她的同事们阐明了细胞质中另一个有趣的现象。科学家们知道,存在于血液中并被T细胞吸收的类风湿性关节炎,会通过一种叫做细胞维甲酸结合蛋白2 (CRABP2)的分子进一步运输到细胞核。细胞质中的CRABP2与RA结合并携带RA进入细胞核,在细胞核中激活核RARα。
研究人员发现,没有CRABP2, RA留在T细胞的细胞质中,而不是激活细胞质中的RARα,它干扰细胞质中TCRs激活的RARα并阻断T细胞的激活。结果,T细胞不能再有效地抵抗感染或杀死癌细胞。这种现象好的一面是,RA对细胞质RARα的干扰减少了T细胞的炎症反应。研究人员认为,这一过程可能成为对抗自身免疫性疾病和其他炎症性疾病的重要靶点。
了解TCR信号的后续步骤
这项新研究强调,不仅要了解受体的位置,还要了解它的特殊才能和相互作用的伙伴。
“视黄酸受体确实是‘复杂的形成者’,这完全取决于它们招募或拒绝谁。它们具有独特的结合分子和释放其他分子的能力,”Cheroutre说。视黄酸受体是复合物的‘建筑师’。”
目前的研究主要集中在T细胞上,但它可能对理解许多其他细胞类型的信号传导有启示。例如,Cheroutre实验室已经进一步证明了这种RARα亚型在癌细胞细胞质中的过度表达。核外RARα在那里做什么?它帮助传递什么信号?
Cheroutre说:“了解这种受体的作用对研究保护性免疫、抗癌治疗、自身免疫性疾病和神经系统疾病具有重要意义。”
Myers实验室将率先开展这项研究的下一步工作。Myers希望弄清楚RARα在TCR/ZAP70信号复合体中的确切作用。“它会调节信号的强度或持续时间吗?”信号的变化是如何传播到基因表达和T细胞活性的?他问道。他的实验室计划使用“系统生物化学”方法进一步研究细胞质和核RARα在T细胞活化和分化中的作用。
Myers说:“最终的目标是看看我们是否能找到一种新的途径,或一组新的途径,可以用来控制自身免疫性疾病和炎症,或增强保护性免疫,以根除肿瘤或对抗感染。”
[1] A regulatory circuit controlled by extranuclear and nuclear retinoic acid receptor α determines T cell activation and function
摘要:T细胞有一种核受体,它的作用非常奇怪——但非常重要——帮助T细胞对抗病原体和摧毁癌细胞。
根据发表在《Immunity》杂志上的一项新研究,T细胞有一种核受体,它的作用非常奇怪——但非常重要——帮助T细胞对抗病原体和摧毁癌细胞。这种受体被称为视黄酸受体α (RARα),已知控制细胞核内的基因表达程序,但它现在似乎也在细胞核外运作,协调细胞表面触发的导致T细胞活化的早期事件。

图1 视黄酸受体α (RARα)帮助T细胞对抗病原体和摧毁癌细胞
科学家们通常不会期望看到像RARα这样的核受体在细胞核外发挥这种作用。然而,新的发现表明,如果细胞质中没有一种形式的RARα, T细胞就无法开始对抗疾病。
“细胞质视黄酸受体是T细胞连接细胞表面感应与下游信号级联和基因表达程序的中心,将T细胞转化为活跃的战斗机,”Hilde Cheroutre教授说。
这项研究也是日本理研综合医学科学中心的科学家、加州大学圣地亚哥分校和索尔克研究所的当地团队成功合作的结果。
帮助T细胞应对危险
为了理解这一发现,它有助于描绘T细胞的地理位置。细胞核(与其捆绑的DNA)位于细胞的中间。被称为细胞器的其他分子和细胞结构漂浮在细胞核外的细胞质中,细胞质被细胞边缘的膜(细胞膜)包围。
被称为T细胞受体(TCRs)的特殊分子位于细胞膜上,在那里它们接收来自其他细胞的信息。你可以把TCRs想象成火灾观测者,从荒野中遥远的小木屋中扫描烟雾的瞭望者。就像火灾侦察员需要提醒官员注意远处的烟雾一样,如果TCRs检测到潜在的威胁,比如病毒或癌细胞,它们需要迅速向总部——细胞核发出信号。
将信号发送到细胞核对于激活基因表达将T细胞转化为战斗细胞至关重要。但TCRs不能只是接电话,那么它们是如何提醒远处的细胞核有麻烦的呢?
信号传递的过程令人着迷。一旦TCR被触发,被称为激酶的分子(将磷酸盐添加到蛋白质上的酶)与接头一起工作,接头告诉附近的蛋白质“点击”在一起,并组装一个特殊的分子“激活复合物”。这种复合物被称为TCR信号体,它在细胞膜内聚集。Cheroutre说:“TCR信号体对于调解细胞内外之间的通信非常重要。”
虽然TCR信号体已经被许多人研究了许多年,但在此之前还没有人在这个激活复合体中检测到RARα。
“这个新发现将改变我们对TCR信号的看法,”Kronenberg说。
揭示RARα的作用
RARα的秘密得以曝光,要归功于CRISPR技术的发展、成像和质谱技术的进步,以及LJI团队和合作者多年来的辛勤工作。
RARα属于视黄酸受体大家族,通常位于细胞核靶基因的控制区域。这些视黄酸受体招募抑制因子和激活因子分子,让它们“关闭”或“打开”这些靶基因的表达。视黄酸受体在细胞核中的这一重要作用为其赢得了“核受体”的称号。
几年前,Cheroutre和她的同事发表了一项研究,表明我们从维生素A中获得的视黄酸(RA)触发核RARα和基因表达,这对抑制调节性T细胞的分化很重要,从而降低免疫反应。
在这项新的研究中,Cheroutre想要研究维甲酸是如何控制这种抑制性T细胞的命运的,所以她的实验室开始更密切地研究维甲酸受体,比如RARα。
研究人员很感兴趣地发现RARα实际上有两种变体,称为同种异构体。“这些同工异构体由相同的基因编码,但它们在一端有一点不同。然而,其结果更为显著,将一种形式锁定在细胞质中,而另一种形式则被限制在细胞核中。”
这两种亚型在T细胞中扮演不同的角色吗?仔细观察后,研究人员意识到这种RARα异构体对维甲酸没有反应,甚至没有合适的设备来充当核受体。
“它没有对核受体很重要的工具,即与DNA相互作用的能力,以及从细胞质转移到细胞核的能力,”Cheroutre说。

利用CRISPR基因编辑技术调节这两种异构体的表达,研究人员发现,调节细胞质异构体会对细胞质中的TCR信号传导造成重大问题,并损害与细胞核控制中心的通信。
RARα在正确的时间出现在正确的位置
一旦他们知道在哪里寻找RARα同种异构体,研究人员就试图找出RARα与其他蛋白质的相互作用。这项工作揭示了与激酶ZAP70的相互作用,ZAP70是TCR信号体的主要成分。
另一个重要的早期线索是,RARα在细胞核外发挥作用,来自Myers实验室领导的蛋白质组学研究。研究人员使用质谱技术检测磷酸化过程,这是一个称为磷酸化基团的分子通过上游激酶附着在蛋白质上的过程。
对T细胞来说,当威胁临近时,磷酸化会刺激关键蛋白发挥作用。“在T细胞刺激的第一个小时左右,会发生成百上千个动态磷酸化事件,”Myers说。
当Myers和他的同事检查他们的数据时,他们惊讶地发现了与RARα相关的磷酸化事件。事实上,RARα的磷酸化在T细胞激活3分钟后就开始了。Myers说:“因为这个事件发生得很早,我们的发现表明RARα的磷酸化在T细胞受体附近,在TCR受到刺激后,它的活性就会爆发。”
这一发现进一步证明RARα的细胞质同工型是由TCR激活的,而不是像核RARα那样由RA激活。因此,这种新形式的RARα代表了细胞表面TCR/ZAP70激活复合物的重要组成部分。
然后,Cheroutre和她的同事们阐明了细胞质中另一个有趣的现象。科学家们知道,存在于血液中并被T细胞吸收的类风湿性关节炎,会通过一种叫做细胞维甲酸结合蛋白2 (CRABP2)的分子进一步运输到细胞核。细胞质中的CRABP2与RA结合并携带RA进入细胞核,在细胞核中激活核RARα。
研究人员发现,没有CRABP2, RA留在T细胞的细胞质中,而不是激活细胞质中的RARα,它干扰细胞质中TCRs激活的RARα并阻断T细胞的激活。结果,T细胞不能再有效地抵抗感染或杀死癌细胞。这种现象好的一面是,RA对细胞质RARα的干扰减少了T细胞的炎症反应。研究人员认为,这一过程可能成为对抗自身免疫性疾病和其他炎症性疾病的重要靶点。
了解TCR信号的后续步骤
这项新研究强调,不仅要了解受体的位置,还要了解它的特殊才能和相互作用的伙伴。
“视黄酸受体确实是‘复杂的形成者’,这完全取决于它们招募或拒绝谁。它们具有独特的结合分子和释放其他分子的能力,”Cheroutre说。视黄酸受体是复合物的‘建筑师’。”
目前的研究主要集中在T细胞上,但它可能对理解许多其他细胞类型的信号传导有启示。例如,Cheroutre实验室已经进一步证明了这种RARα亚型在癌细胞细胞质中的过度表达。核外RARα在那里做什么?它帮助传递什么信号?
Cheroutre说:“了解这种受体的作用对研究保护性免疫、抗癌治疗、自身免疫性疾病和神经系统疾病具有重要意义。”
Myers实验室将率先开展这项研究的下一步工作。Myers希望弄清楚RARα在TCR/ZAP70信号复合体中的确切作用。“它会调节信号的强度或持续时间吗?”信号的变化是如何传播到基因表达和T细胞活性的?他问道。他的实验室计划使用“系统生物化学”方法进一步研究细胞质和核RARα在T细胞活化和分化中的作用。
Myers说:“最终的目标是看看我们是否能找到一种新的途径,或一组新的途径,可以用来控制自身免疫性疾病和炎症,或增强保护性免疫,以根除肿瘤或对抗感染。”
[1] A regulatory circuit controlled by extranuclear and nuclear retinoic acid receptor α determines T cell activation and function



